题目内容
1.维生素C是一种水溶性维生素(其水溶液呈酸性),它的化学式是C6H8O6,人体缺乏这样的维生素能得坏血症,所以维生素C又称抗坏血酸.在新鲜的水果、蔬菜、乳制品中都富含维生素C,例如新鲜橙汁中维生素C的含量在500mg/L左右.某校课外活动小组测定了某牌子的软包装橙汁中维生素C的含量,下面是测定实验分析报告.(请填写有关空白)(一)测定目的:测定××牌软包装橙汁中维生素C的含量.
(二)测定原理:C6H8O6+I2→C6H6O6+2H++2I-
(三)实验用品及试剂:
(1)仪器和用品(自选,略)
(2)试剂:指示剂淀粉溶液(填名称),浓度为7.50×10-3mol•L-1的I2标准溶液、蒸馏水等.
(四)实验过程:
(1)洗涤仪器,检查滴定管是否漏液,润洗后装好标准碘溶液待用.
(2)用 (填仪器名称)向锥形瓶中移入20.00mL待测橙汁,滴入2滴指示剂.用左手控制滴定管的活塞(填部位),右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化,直到滴定终点.滴定至终点时的现象是最后一滴标准液滴入,溶液由无色变为蓝色,且半分钟不褪色.
(五)数据记录与处理:
若滴定中消耗标准碘溶液的体积是15.00mL,则此橙汁中维生素C的含量是990mg/L.
(六)问题讨论:
从分析数据看,此软包装橙汁是否是纯天然橙汁?不是,(填“是”或“不是”或“可能是”).
制造商最可能采取的做法是C(填编号):
A.加水稀释天然橙汁 B.橙汁已被浓缩 C.将维生素C作为添加剂.
分析 (三)(2)根据碘能使淀粉变蓝色选择试剂;
(四)(2)橙汁呈酸性,用酸式滴定管取用;定时左手控制活塞;根据反应的原理,当出现溶液变蓝色且半分钟内不褪色时,维生素C已全部参加了反应;
(五)数值记录和处理可以记录每次实验数据,起始、终了、变化的体积,根据反应原理及题中有关数据,可以计算出橙汁中维生素C的含量;
(六)新鲜橙汁中维生素C的含量在500mg/L左右分析判断;
解答 解:(三)(2)利用I2氧化维生素C,根据碘使淀粉显蓝色的性质,应选择淀粉溶液作指示剂,
故答案为:淀粉溶液;
(四)(2)橙汁呈酸性,用酸式滴定管取用,向锥形瓶中移入20.00mL待测橙汁,滴入2滴指示剂;
在滴定时左手控制活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化直到滴定终点;根据反应的原理,当出现溶液变蓝色时,维生素C已全部参加了反应,滴定终点现象为:最后一滴标准液滴入,溶液由无色变为蓝色,且半分钟不褪色,
故答案为:酸式滴定管;活塞;锥形瓶中溶液颜色的变化;最后一滴标准液滴入,溶液由无色变为蓝色,且半分钟不褪色;
(五)15ml标准碘溶液含有碘的质量为:254g/mol×0.015L×7.5×10-3mol•L-1=28.575mg
设20.0mL待测橙汁中维生素C的质量为X
C6H8O6+I2→C6H6O6+2H++2I-
176 254
X 28.575mg
$\frac{176}{254}=\frac{X}{28.575mg}$,
解得:X=19.8mg
则1L中含维生素C的质量为:19.8mg×1000ml/20ml=990mg,
所以,则此橙汁中维生素C的含量是990mg/L,
故答案为:990;
(六)新鲜橙汁中维生素C的含量在500mg/L左右分析判断,从分析数据看此橙汁中维生素C的含量是990mg/L,此软包装橙汁不是纯天然橙汁,可能采取的做法是将维生素C作为添加剂,故选C;
故答案为:不是,C.
点评 本题考查了橙汁中维生素C的含量,属于综合实验题,完成本题时要注意题中数据的处理,合理进行误差的分析等,本题难度中等.

| 容器编号 | 起始时各物质物质的量/mol | 达到平衡时体系能量的变化 | ||
| A | B | C | ||
| ① | 2 | 1 | 0 | 0.75Q kJ |
| ② | 0.4 | 0.2 | 1.6 | |
| A. | 容器①、②中反应的平衡常数均为4 | |
| B. | 容器②中达到平衡时放出的热量为0.05QkJ | |
| C. | 向容器①中通入氦气,平衡时A的转化率不变 | |
| D. | 其他条件不变,若容器②保持恒容绝热,则达到平衡时C的体积分数小于$\frac{2}{3}$ |
| A. | FeCl3溶液能止血和面粉厂的静电除尘都是利用了胶体的聚沉性质 | |
| B. | 除去锅炉水垢中的CaSO4,可先使用碳酸钠溶液浸泡处理,最后用酸除去 | |
| C. | 大量排放SO2、NO2和CO2都会导致酸雨的形成 | |
| D. | 工业上用NaOH与氯气反应制取漂白粉 |
| A. | v(Fe)=0.5 mol/(L•min) | B. | v(H2SO4)=1 mol/(L•min) | ||
| C. | v(H2SO4)=0.5 mol/(L•min) | D. | v(FeSO4)=1 mol/(L•min) |
| A. | CH3CH2CH2CH3(3组) | B. | CH2═CH-CH2CH3(2组) | ||
| C. | 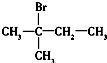 (4组) (4组) | D. | 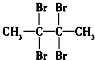 (1组) (1组) |
| A. | 70℃,将0.1mol 镁粉加入到10mL 6mol•L-1 的硝酸溶液中 | |
| B. | 60℃,将0.2mol 镁粉加入到20mL 3mol•L-1 的盐酸溶液中 | |
| C. | 60℃,将0.1mol 镁粉加入到10mL 3mol•L-1 的硫酸溶液中 | |
| D. | 60℃,将0.2mol 铁粉加入到10mL 3mol•L-1 的盐酸溶液中 |
| A. | NaAlO2溶液中通入过量的CO2:2 AlO2-+3H2O+CO2═2Al(OH)3↓+CO32- | |
| B. | 磨口玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH-═Na2SiO3↓+H2O | |
| C. | 向海带灰浸出液中加入稀硫酸、双氧水:2I-+2H++H2O2═I2+2H2O | |
| D. | NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3-+OH-+Ba2+═H2O+BaCO3↓ |
| A. | 150mL 1mol/L的NaCl溶液 | B. | 75mL 1mol/L的FeCl3溶液 | ||
| C. | 150mL 0.5mol/L的MgCl2溶液 | D. | 75mL 2mol/L的NH4Cl溶液 |