题目内容
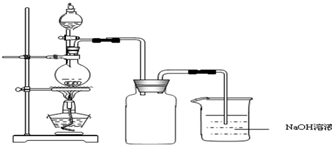
硫酸铜是一种应用极其广泛的化工原料.制备硫酸铜是无机化学实验教学中一个重要的实验.由于铜不能与稀硫酸直接反应,实验中将浓硝酸分次加入到铜粉与稀硫酸中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图1、2所示).
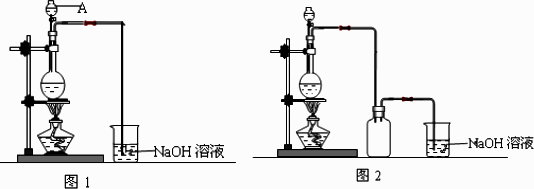
(1)图2是图1的改进装置,改进的目的是________.
(2)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:空气为氧化剂法
方案1:以空气为氧化剂.将铜粉在仪器B中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应.
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应.向反应液中加FeSO4或Fe2(SO4)3,反应完全后,向其中加物质甲调节pH到3~4,产生Fe(OH)3沉淀,过滤、蒸发、结晶,滤渣作催化剂循环使用.
(已知Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为3.7、6.4.)
请回答下列问题:
①方案1中的B仪器名称是________.
②方案2中甲物质是________(填字母序号).
a、CaO b、CuCO3 c、CaCO3
第二组:过氧化氢为氧化剂法
将3.2 g铜丝放到45 mL 1.5 mol/L的稀硫酸中,控温在50℃.加入18 mL 10%的H2O2,反应0.5 h后,升温到60℃,持续反应1 h后,过滤、蒸发结晶、减压抽滤等,用少量95%的酒精淋洗后晾干,得CuSO4·5H2O 10.6 g.请回答下列问题:
③该反应的离子反应方程式为________.
④控制温度在50℃和60℃加热的原因为________,晶体采用酒精淋洗的优点是________.
⑤上述两种氧化法中,更符合绿色化学理念的是________(填“第一组”或“第二组”),理由是________.
解析:
|
(1)安全瓶(防止倒吸等)(2分) (2)①坩埚(2分) ②b(2分) ③Cu+H2O2+2H+ ④防止双氧水分解(2分),酒精与水互溶且极易挥发,减少晶体溶解(2分), ⑤第二组(2分) 理由:第一组中的方案1需要加热,消耗能源,方案2所得产品含有铁元素杂质.而第二组方案几乎不产生有害气体,且所得产品纯度较高.(2分) |

 阅读快车系列答案
阅读快车系列答案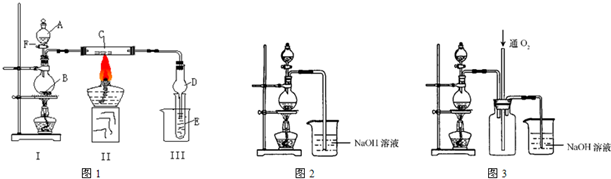
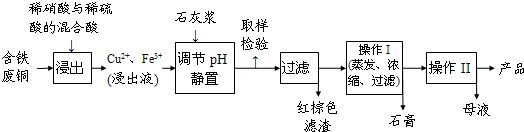
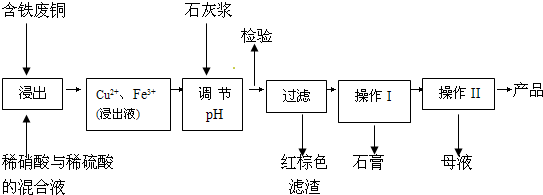
 硫酸铜是一种应用极其广泛的化工原料.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示).
硫酸铜是一种应用极其广泛的化工原料.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示).