题目内容
5.A、E为1-18号元素中的某单质,B、C为其化合物,它们之间的转化关系如图所示:A$\stackrel{E}{→}$B$\stackrel{E}{→}$C若C溶于水能产生强酸,回答下列问题,写出符合题意的两种情况(请写化学式).
第一种情况:AS;BSO2;CSO3;
第二种情况:AN2;BNO;CNO2.
分析 A、E为1-18号元素中的某单质,B、C为其化合物,能连续与E反应,E应为O2,则B、C应为氧化物,短周期元素形成的氧化物中,常见能溶于水能产生强酸的常见氧化物有SO3或NO2,以此推断可解答该题.
解答 解:A、E为1-18号元素中的某单质,B、C为其化合物,能连续与E反应,E应为O2,则B、C应为氧化物,短周期元素形成的氧化物中,常见能溶于水能产生强酸的常见氧化物有SO3或NO2,
当C为SO3时,A为S,B为SO2,
当C为 NO2时,A为N2,B为NO.
故答案为:第一种情况:S,SO2,SO3;第二种情况:N2,NO,NO2.
点评 本题考查无机物的推断,题目难度不大,本题注意短周期元素形成的氧化物中能与水反应的物质,此为解答该题的关键.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
20.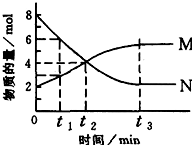 在一定温度下,某容器内某一反应中,M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,某容器内某一反应中,M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
 在一定温度下,某容器内某一反应中,M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,某容器内某一反应中,M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A. | 此反应为不可逆反应 | B. | t2时,正逆反应速率相等,达到平衡 | ||
| C. | t3时,正反应速率大于逆反应速率 | D. | t3时,正反应速率等于逆反应速率 |
17.醋酸的电离方程式为CH3COOH(aq)?H+(aq)+CH3COO-(aq)△H>0.25℃时,0.1mol/L醋酸溶液中存在下述关系:$\frac{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=1.75×10-5,其中的数值是该温度下醋酸的电离平衡常数(Ka).下列说法正确的是( )
| A. | 向该溶液中滴加几滴浓盐酸,平衡逆向移动,c(H+)减小 | |
| B. | 向该溶液中加入少量CH3COONa固体,平衡正向移动 | |
| C. | 该温度下0.01mol/L醋酸溶液Ka<1.75×10-5 | |
| D. | 升高温度,c(H+)增大,Ka变大 |
14.为除去C2H4中混有的SO2,可将混合气体通过( )
| A. | 酸性高锰酸钾溶液 | B. | 溴水 | ||
| C. | Na2CO3溶液 | D. | NaOH溶液 |
7.把500mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀.则该混合溶液中钾离子浓度为( )
| A. | 0.1(b-2a)mol•L-1 | B. | 10(2a-b)mol•L-1 | C. | 10(b-a)mol•L-1 | D. | 10(b-2a)mol•L-1 |

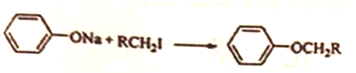

 .
.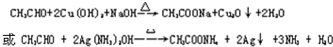 .
.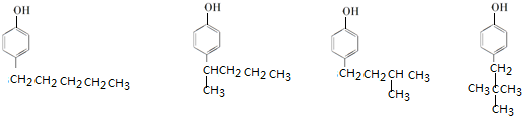 、
、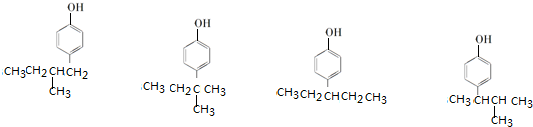 (其中任意两种).
(其中任意两种).