题目内容
下列反应中HNO3既表现出酸性又表现出强氧化性的是( )
| A、稀硝酸与Fe2O3反应 |
| B、稀硝酸与NaOH溶液反应 |
| C、浓硝酸与灼热的碳反应 |
| D、浓硝酸与铜反应 |
考点:硝酸的化学性质
专题:氮族元素
分析:硝酸表现氧化性,则反应后N元素的化合价降低;表现出酸性,反应物中有硝酸盐生成.
解答:
解:A.稀硝酸与Fe2O3反应反应生成硝酸铁和水,化合价没有变化,不是氧化还原反应,硝酸只表现出酸性,故A错误;
B.稀硝酸与NaOH溶液反应生成硝酸钠和水,化合价没有变化,不是氧化还原反应,硝酸只表现出酸性,故B错误;
C.浓硝酸与灼热的碳反应生成二氧化碳、二氧化氮和水,硝酸只表现出强氧化性,故C错误;
D.浓硝酸与铜反应生成硝酸铜、NO和水,N元素化合价降低,硝酸表现出氧化性,生成硝酸铜,硝酸还表现出酸性,故D正确;
故选D.
B.稀硝酸与NaOH溶液反应生成硝酸钠和水,化合价没有变化,不是氧化还原反应,硝酸只表现出酸性,故B错误;
C.浓硝酸与灼热的碳反应生成二氧化碳、二氧化氮和水,硝酸只表现出强氧化性,故C错误;
D.浓硝酸与铜反应生成硝酸铜、NO和水,N元素化合价降低,硝酸表现出氧化性,生成硝酸铜,硝酸还表现出酸性,故D正确;
故选D.
点评:本题考查硝酸的性质,难度不大.注意硝酸酸性与氧化性的判断.

练习册系列答案
相关题目
已知某溶液中只存在OH-、Cl-、NH4+、H+四种离子,下列说法不正确的是( )
| A、若溶液中c(NH4+)=c(Cl-),则该溶液一定显中性 |
| B、若溶液中c(NH4+)>c(Cl-)>c(OH-)>c(H+),则溶液中一定含有NH4Cl和NH3?H2O |
| C、若溶液中c(Cl-)>c(NH4+)>c(H+)>c(OH-),则溶液中可能含有NH4Cl或可能含有NH4Cl和HCl |
| D、若溶液中c(Cl-)>c(H+)>c(NH4+)>c(OH-),则溶液中含有大量的NH4Cl和少量的HCl |
下列微粒的结构示意图中氧离子结构示意图的是( )
A、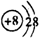 |
B、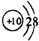 |
C、 |
D、 |
金属晶体具有延展性的原因是( )
| A、金属阳离子之间存在斥力 |
| B、金属原子半径都较大,价电子较少 |
| C、金属中大量自由电子受到外力作用时,运动速度加快 |
| D、金属受到外力作用时,各原子层容易发生相对滑动,但不会改变原来的排列方式,也不会破坏金属键 |
下列有机物的命名正确的是( )
| A、3,3-二甲基丁烷 |
| B、3-甲基-2-乙基戊烷 |
| C、2,3-二甲基-1-戊烯 |
| D、2-甲基-1-戊炔 |
下列物质性质变化规律正确的是( )
| A、金属Na、Mg、Al的硬度依次降低 |
| B、O、F、H的原子半径依次减小 |
| C、干冰、钠、冰的熔点依次降低 |
| D、HI、HBr、HCl的熔点依次升高 |
互为同分异构体的一组物质是( )
| A、H2O和H2O2 |
| B、35Cl和37Cl |
| C、氧气(O2)与臭氧(O3) |
| D、乙醇(CH3CH2OH)和甲醚(CH3OCH3) |
有主族元素X、Y,X的原子序数为a,X+比Y2-少8个电子,则Y的原子序数为( )
| A、a+4 |
| B、a+5 |
| C、a+6 |
| D、a+7 |