题目内容
12.在25℃时,某溶液中,由水电离出的c(H+)=1×10-12mol/L,则该溶液的pH可能是( )| A. | 12 | B. | 7 | C. | 6 | D. | 2 |
分析 在25℃时,某溶液中,由水电离出的c(H+)水=1.0×10-12 mol/L<10-7mol/L,说明该溶液中的溶质抑制水的电离,溶质能电离出氢离子、氢氧根离子就能抑制水电离,据此分析判断.
解答 解:25℃时:Kw=c(OH-)×c(H+)=10-14,纯水中c(H+)=c(OH-)=1.0×10-7 mol/L,在25℃时,某溶液中,由水电离出的c(H+)水=1.0×10-12 mol/L<10-7mol/L,说明该溶液中的溶质抑制水的电离,溶质能电离出氢离子、氢氧根离子就能抑制水电离,则该溶质可能是酸或碱或强酸的酸式盐,如果为酸溶液,则pH=2,如果为盐溶液,则pH=12,故选AD.
点评 本题涉及pH的简单计算,明确溶液中的溶质是抑制水电离是解本题的关键,能电离出氢离子或氢氧根离子的物质抑制水电离,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.A(g)+B(g)?3C(g),图中甲、乙、丙分别表示在不同的条件下生成物C在反应混和物中的百分含量(C%)和反应时间(t)的关系.有关图象的说法正确的是( )
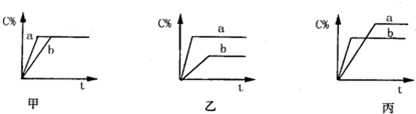

| A. | 若甲图中两条曲线分别表示有催化剂和无催化剂时的情况,则b表示有催化剂的情况 | |
| B. | 若乙图中a曲线表示200℃、b曲线表示100℃时的情况,则反应的正反应是放热反应 | |
| C. | 若丙图中两条曲线分别表示不同压强下的情况,则b曲线是表示压强较大的情况 | |
| D. | 若丙图中两条曲线分别表示不同温度下的情况,则a曲线是表示温度较大的情况 |
3. 2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢,并采用新一代的氮化镓铟高亮度LED材料.下列有关说法正确的是( )
2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢,并采用新一代的氮化镓铟高亮度LED材料.下列有关说法正确的是( )
 2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢,并采用新一代的氮化镓铟高亮度LED材料.下列有关说法正确的是( )
2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢,并采用新一代的氮化镓铟高亮度LED材料.下列有关说法正确的是( )| A. | 合金的熔点通常比组分金属高,硬度比组分金属小 | |
| B. | 已知Ga处于ⅢA族,可推知氮化镓化学式为Ga3N2 | |
| C. | 用金属铝与V2O5冶炼钒,铝作还原剂 | |
| D. | 合金的化学性质一般与其各成分金属的化学性质不同 |
20.X、Y两元素是元素周期表中前20号元素,原子序数X比Y大,其简单离子的电子层结构相同.请判断下列说法正确的是( )
| A. | X和Y一定是不同周期元素,但可能是同一主族元素 | |
| B. | 若X和Y都为金属,则X的金属性比Y强 | |
| C. | 若X、Y的简单离子分别是aXm+和bYn-,则有a+m=b-n | |
| D. | 若X和Y都为非金属,则它们的氢化物的稳定性X比Y强. |
7.下列溶液中一定呈中性的是( )
| A. | pH=7的溶液 | B. | c(H+)=c(OH-)=10-6mol•L-1的溶液 | ||
| C. | 能够与Na反应生成H2的溶液 | D. | 电解食盐水最后所得溶液 |
17.常温下,下列各组物质不能用一种试剂通过化学反应区别的是( )
| A. | 苯 乙酸乙酯 乙醇 | B. | AgNO3 KNO3 Na2CO3 | ||
| C. | MnO2 CuO FeO | D. | (NH4)2SO4 K2SO4 NH4Cl |
4.下列分类不正确的是( )
| A. | 熔融的氯化钠是电解质 | |
| B. | 盐酸溶液属于非电解质 | |
| C. | 雾属于胶体,当用激光笔照射时,可以看到丁达尔现象 | |
| D. | 置换反应一定属于氧化还原反应 |
1.下列实验均发生了化学反应:①将铁钉放入CuSO4溶液中;②向FeSO4溶液中滴加稀硝酸;③将铜丝放入FeCl3溶液中.下列判断中,正确的是( )
| A. | 上述实验证明了氧化性:Fe3+>Fe2+>Cu2+ | |
| B. | 上述实验证明了Fe2+既有氧化性又有还原性 | |
| C. | 实验①中的化学反应是置换反应 | |
| D. | 向三个实验后的溶液中加入足量NaOH溶液振荡,最终都有Fe(OH)3生成 |
2.下列叙述不正确的是( )
| A. | 把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 | |
| B. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 | |
| C. | 原电池中电流由正极流向负极,阳离子向正极移动 | |
| D. | 用惰性电极电解AgNO3溶液一段时间后,加入一定质量Ag粉,溶液能恢复原状 |