题目内容
20.X、Y两元素是元素周期表中前20号元素,原子序数X比Y大,其简单离子的电子层结构相同.请判断下列说法正确的是( )| A. | X和Y一定是不同周期元素,但可能是同一主族元素 | |
| B. | 若X和Y都为金属,则X的金属性比Y强 | |
| C. | 若X、Y的简单离子分别是aXm+和bYn-,则有a+m=b-n | |
| D. | 若X和Y都为非金属,则它们的氢化物的稳定性X比Y强. |
分析 X、Y两元素是元素周期表中前20号元素,原子序数X比Y大,其简单离子的电子层结构相同,离子核外电子数相同.若X、Y均为阳离子或均为阴离子时,处于同周期,若为阴阳离子时,X处于Y的下一周期,且X为金属元素、Y为非金属性元素.
A.X、Y均为阳离子或均为阴离子时,可能处于同周期,同主族元素离子不可能具有相同电子层结构;
B.若X和Y都为金属,二者只能同周期,原子序数越大,金属性越弱;
C.根据核外电子数相同计算判断,离子核外电子数=质子数-所带电荷;
D.若X和Y都为非金属,二者只能同周期,非金属性越强,氢化物越稳定.
解答 解:X、Y两元素是元素周期表中前20号元素,原子序数X比Y大,其简单离子的电子层结构相同,离子核外电子数相同.若X、Y均为阳离子或均为阴离子时,处于同周期,若为阴阳离子时,X处于Y的下一周期,且X为金属元素、Y为非金属性元素.
A.X、Y均为阳离子或均为阴离子时,可能处于同周期,同主族元素离子不可能具有相同电子层结构,故A错误;
B.若X和Y都为金属,二者只能同周期,原子序数越大,金属性越弱,故金属性X<Y,故B错误;
C.离子核外电子数相等,则a-m=b-(-n),即a-m=b+n,故C错误;
D.若X和Y都为非金属,二者只能同周期,X原子序数较大,故X的非金属性较强,故氢化物的稳定性X比Y强,故D正确,
故选:D.
点评 本题考查结构性质位置关系应用,侧重对元素周期律的考查,关键是确定元素的相等位置,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.下列各项中表达正确的是( )
| A. | 硫的周期位置:第3周期ⅣA族 | B. | F-的结构示意图: | ||
| C. | 氨的电子式: | D. | 用电子式表示KI的形成过程: |
5.某溶液里存有NH4+ Fe3+ Cu2+ Cl- SO42-离子,溶液不浑浊的是( )
| A. | CuCl2 NH4Cl Fe2(SO4)3 NaNO3 | |
| B. | (NH4)2SO4 CuSO4 Na2CO3 FeCl3 | |
| C. | Cu(NO3)2 NH4NO3 FeCl3 H2S | |
| D. | Ba Cl2 Cu(NO3)2 (NH4)2SO4 Fe (NO3)3 |
12.在25℃时,某溶液中,由水电离出的c(H+)=1×10-12mol/L,则该溶液的pH可能是( )
| A. | 12 | B. | 7 | C. | 6 | D. | 2 |
9.下列说法不正确的是( )
| A. | 对“地沟油”蒸馏可以获得汽油等燃料 | |
| B. | 不法分子制作假鸡蛋用的海藻酸钠、氯化钙以及碳酸钙都属于盐 | |
| C. | 明矾用于净水既与盐类的水解有关,又与胶体的性质有关 | |
| D. | FeS难溶于水(Ksp=1.6×10-19),但能除去水中的Cu2+[已知Ksp(CuS)=6.3×10-36] |
10.下列说法中,不正确的是( )
| A. | 天然气的主要成分是甲烷 | |
| B. | 将固体燃料粉碎可以提高燃料的燃烧效率 | |
| C. | 废弃的镍镉电池如不回收,会严重污染环境 | |
| D. | 绿色化学的核心就是如何对被污染的环境进行无毒无害的治理 |
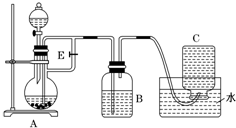 如图所示装置可用来制取Fe(OH)2和观察Fe(OH)2在空气中被氧化时的颜色变化.实验时必须使用铁屑、6mol•L-1硫酸溶液,其他试剂任选.填写下列空白:
如图所示装置可用来制取Fe(OH)2和观察Fe(OH)2在空气中被氧化时的颜色变化.实验时必须使用铁屑、6mol•L-1硫酸溶液,其他试剂任选.填写下列空白: ,已知断裂1mol B-B吸收167kJ的热量,生成1mol B≡B放出942kJ热量.试写出由B4气态分子变成B2气态分子的热化学方程式:N4(g)═2N2(g)△H=-882 kJ/mol;
,已知断裂1mol B-B吸收167kJ的热量,生成1mol B≡B放出942kJ热量.试写出由B4气态分子变成B2气态分子的热化学方程式:N4(g)═2N2(g)△H=-882 kJ/mol;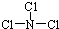 ,X与水反应的化学方程式是NCl3+3H2O═NH3+3HClO;
,X与水反应的化学方程式是NCl3+3H2O═NH3+3HClO;
 +H2O,H中的官能团有氯原子、羟基、醚键(填名称),与E具有相同官能团的E的同分异构体还有
+H2O,H中的官能团有氯原子、羟基、醚键(填名称),与E具有相同官能团的E的同分异构体还有


 (其中任意两个)(任写两个,不考虑立体结构);
(其中任意两个)(任写两个,不考虑立体结构); .
.