题目内容
【题目】常见有机物A~D有下图转化关系(部分反应条件和部分产物已略去)。已知A是一种酯,其分子式为C4H8O2,B是食醋的主要成分。
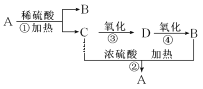
请回答下列问题:
(1)写出C和D含有的官能团名称___________、_____________;
(2)写出B和D的结构简式___________、_____________;
(3)写出B和C生成A的化学方程式___________________________________。
【答案】羟基 醛基 CH3COOH CH3CHO CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
【解析】
A是一种酯,其分子式为C4H8O2,B是食醋的主要成分,则B为乙酸,C为乙醇,乙酸和乙醇发生酯化反应生成A,A为乙酸乙酯;C氧化生成D,D氧化生成B,乙醇D为乙醛,据此分析解答。
根据上述分析,A为乙酸乙酯,B为乙酸,C为乙醇,D为乙醛;
(1) C为乙醇,D为乙醛,含有的官能团分别为羟基和醛基,故答案为:羟基;醛基;
(2) B为乙酸,D为乙醛,结构简式分别为CH3COOH、CH3CHO,故答案为:CH3COOH;CH3CHO;
(3)乙酸和乙醇发生酯化反应生成乙酸乙酯,反应的化学方程式为CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O,故答案为:CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,故答案为:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O。
CH3COOCH2CH3+H2O。

【题目】阅读体检报告呈现的的部分内容,判断下列说法不正确的是
项目名称 | 检查结果 | 单位 | 参考范围 |
钾 | 4.1 | mmol/L | 3.5~5.5 |
钙 | 2.15 | mmol/L | 2.13~2.70 |
胱抑素C | 0.78 | mg/L | 0.59~1.03 |
尿素 | 4.18 | mmol/L | 2.78~7.14 |
甘油三酯 | 1.50 | mmol/L | 0.45~1.70 |
A.体检指标均以物质的量浓度表示
B.表中所示的检查项目均正常
C.尿素是蛋白质的代谢产物
D.甘油三酯的结构可表示为![]() (R1、R2、R3为烃基)
(R1、R2、R3为烃基)