��Ŀ����
����Ŀ����֪:150 ��ʱ�� NO2�����ֽⷴӦ2NO2(g)![]() 2NO(g)+O2(g) ��H>0�����ݻ�Ϊ1 L���ܱ�������ͨ��0.05 mol NO2����150 ��ʱ��ַ�Ӧ���ﵽƽ�����c(NO)=0.04 mol/L��
2NO(g)+O2(g) ��H>0�����ݻ�Ϊ1 L���ܱ�������ͨ��0.05 mol NO2����150 ��ʱ��ַ�Ӧ���ﵽƽ�����c(NO)=0.04 mol/L��
��1����˵��������Ӧ�Ѿ��ﵽƽ��״̬����________(����ĸ)��
A���������������ɫ���ٱ仯
B��������ѹǿ���ٱ仯
C��������������ܶȲ��ٱ仯
D�������������ƽ��Ħ���������ٱ仯
E.v��(NO2)=v��(NO)
F.��ͬʱ���ڣ�ÿ����2��NO2���ӣ���������2��NO����
��2��150 ��ʱ������Ӧ��ƽ�ⳣ��K=________(����ֵ)��
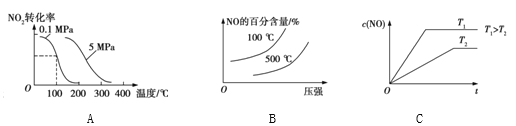
��3�������йظ÷�Ӧ��ͼ������ȷ����__________(����ĸ)��
��4��������������ʱ����(N2H4)��Ϊ�����������ȼ�ϣ�NO2Ϊ����������Ӧ����N2��ˮ��������֪: N2(g)+2O2(g)��2NO2(g) ��H=+67.7 kJ/mol��N2H4(g)+O2(g)��N2(g)+2H2O(g) ��H=-534 kJ/mol��[��Դ��N2H4(g)��NO2��Ӧ���Ȼ�ѧ����ʽΪ___________________________��
��5������500 mL 0.1 mol/L��CH3COONa��Һ�м���250mL 0.1 mol/L��HNO3����ʱ��Һ�����ԣ������û����Һ������Ũ�ȵĴ�С˳��Ϊ___________��
���𰸡���1��ABDE
��2��0.32��3��C
��4��2N2H4(g)+2NO2(g)��3N2(g)+4H2O(g)��H=-1 135.7 kJ/mol
��5��c(Na+)>c(CH3COO-)>c(NO3-)>c(H+)>c(OH-)
��������
�����������1��A���������������ɫ���ٱ仯˵��NO2Ũ�����ٱ仯����Ӧ�ﵽƽ��״̬��A��ȷ��B������Ӧ������ӣ�������ѹǿ���ٱ仯����Ӧ�ﵽƽ��״̬��B��ȷ��C���ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������������ݻ�ʼ���Dz���ģ����������������ܶȲ��ٱ仯����˵����Ӧ�ﵽƽ��״̬��C������D���������ƽ����Է��������ǻ�����������ͻ�������ܵ����ʵ����ı�ֵ���������䣬�����ʵ����DZ仯�ģ����������������ƽ��Ħ���������ٱ仯����˵����Ӧ�ﵽƽ��״̬��D��ȷ��E.v��(NO2)��v��(NO)��ʾ���淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬��E��ȷ��F.��ͬʱ���ڣ�ÿ����2��NO2���ӣ���������2��NO���Ӿ���������Ӧ���ʣ�����˵����F��������ѡABDE��
��2�� 2NO2(g)![]() 2NO(g)+O2(g)
2NO(g)+O2(g)
��ʼŨ�ȣ�mol/L�� 0.05 0 0
ת��Ũ�ȣ�mol/L�� 0.04 0.04 0.02
ƽ��Ũ�ȣ�mol/L�� 0.01 0.04 0.02
����150��ʱ������Ӧ��ƽ�ⳣ��K��![]() ��0.32��
��0.32��
��3��A������Ӧ��������ӵ����ȷ�Ӧ�������¶�NO2ת�������ӣ�A������B������Ӧ�����������¶�ƽ��������Ӧ������У�NO�������ӣ�B������C���¶ȸ߷�Ӧ���ʿ죬����ƽ���ʱ������NO��Ũ�ȴ�C��ȷ����ѡC��
��4����֪:��N2(g)+2O2(g)��2NO2(g) ��H=+67.7 kJ/mol
��N2H4(g)+O2(g)��N2(g)+2H2O(g) ��H=-534 kJ/mol
��������˹���ɿ�֪����2���ټ��õ�
N2H4(g)��NO2��Ӧ���Ȼ�ѧ����ʽΪ2N2H4(g)+2NO2(g)��3N2(g)+4H2O(g)��H=-1135.7 kJ/mol��
��5������500 mL 0.1 mol/L��CH3COONa��Һ�м���250mL 0.1 mol/L��HNO3����Ӧ��������������ƣ�����ʣ��Ĵ�������Ũ����ȡ���ʱ��Һ�����ԣ�˵������ĵ���̶ȴ��ڴ������ˮ��̶ȣ�������û����Һ������Ũ�ȵĴ�С˳��Ϊc(Na+)>c(CH3COO-)>c(NO3-)>c(H+)>c(OH-)��