题目内容
将1 L含有0.4 mol CuSO4和0.2 mol NaCl 的水溶液用惰性电极电解一段时间后。
(1)若在一个电极上得到0.1 mol Cu,另一电极上析出气体(在标准状况下)的体积是________ L。
(2)若在一个电极上恰好得到0.4 mol Cu,另一电极上再析出气体(在标准状况下)的体积是________ L。
(1)若在一个电极上得到0.1 mol Cu,另一电极上析出气体(在标准状况下)的体积是________ L。
(2)若在一个电极上恰好得到0.4 mol Cu,另一电极上再析出气体(在标准状况下)的体积是________ L。
(1)2.24 (2)3.36
(1)设另一电极上析出气体在标准状况的体积为x,根据题意得,在另一电极上得到的气体全是Cl2,电解方程式为:
Cu2++2Cl- Cu + Cl2↑
Cu + Cl2↑
1 mol 22.4 L。
0.1 mol x
x=2.24 L。
(2)当再析出另外0.3 mol Cu时,其阳极反应为:
4OH--4e-=2H2O+O2↑
即2Cu~ 4e- ~ O2
n(O2)=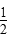 n(Cu)=0.15 mol,
n(Cu)=0.15 mol,
V(O2)=0.15 mol×22.4L·mol-1=3.36L。
Cu2++2Cl-
 Cu + Cl2↑
Cu + Cl2↑1 mol 22.4 L。
0.1 mol x
x=2.24 L。
(2)当再析出另外0.3 mol Cu时,其阳极反应为:
4OH--4e-=2H2O+O2↑
即2Cu~ 4e- ~ O2
n(O2)=
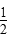 n(Cu)=0.15 mol,
n(Cu)=0.15 mol,V(O2)=0.15 mol×22.4L·mol-1=3.36L。

练习册系列答案
相关题目