题目内容
下列电子式书写正确的是
A.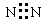 | B. | C.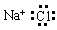 | D.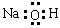 |
B
解析试题分析:A.N2分子中的每个N原子上还有一对电子对,电子式是: ;错误;B.H2O分子中H原子与O原子间通过共用电子对结合,电子式是
;错误;B.H2O分子中H原子与O原子间通过共用电子对结合,电子式是  ,正确;C.NaCl是离子化合物,微粒间以离子键结合,电子式是:
,正确;C.NaCl是离子化合物,微粒间以离子键结合,电子式是: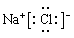 ;错误;D.NaOH是离子化合物,阳离子和阴离子通过离子键结合,电子式是:
;错误;D.NaOH是离子化合物,阳离子和阴离子通过离子键结合,电子式是: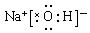 ,错误;
,错误;
考点:考查电子式书写正误判断的知识。

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
在以离子键为主的化学键中常含有共价键的成分。下列各组原子形成化学键中共价键成分最少的是( )
| A.Li,F | B.Na,Cl | C.Na,F | D.Mg,O |
下列物质中,中心原子的杂化类型为sp3杂化的是
| A.C2H6 | B.C2H2 | C.BF3 | D.C2H4 |
下列变化过程中,化学键没有被破坏的是
| A.HCl溶于水 | B.干冰升华 |
| C.固体NaCl熔融 | D.煤矿中瓦斯(主要成分CH4)遇火爆炸 |
下列说法正确的是
| A.由分子构成的物质一定含有共价键 |
| B.由非金属元素组成的化合物不一定是共价化合物 |
| C.非极性键只存在于双原子单质分子中 |
| D.不同元素组成的多原子分子中的化学键一定都是极性键 |
意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的气态N4分子,其分子结构如图所示。已知断裂1mol N-N吸收167kJ热量,生成1 mol N≡N放出942kJ热量,根据以上信息判断,下列说法正确的是
| A.1mol N4转变成N2将放出882kJ热量 | B.N4属于一种新型的化合物 |
| C.N4与N2互为同分异构体 | D.N4是由极性键组成的分子 |
下列各组微粒属于等电子体的是( )
| A.CO和CO2 | B.NO和NO2 | C.CH4和NH3 | D.CO2和N2O |
下列说法不正确的是
| A.乙烯、苯、溴苯分子中的所有原子均共平面 |
| B.水加热至1000℃以上才分解是因为水分子间存在着氢键 |
| C.常温下浓硫酸和浓硝酸能使铝发生钝化,所以可以用铝槽罐车运输浓硫酸、浓硝酸 |
| D.能发生银镜反应的有机物结构中一定含有-CHO |
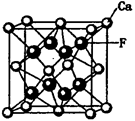
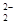 存在,使晶胞沿一个方向拉长,则CaC2晶体中1个C
存在,使晶胞沿一个方向拉长,则CaC2晶体中1个C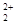 互为等电子体,O
互为等电子体,O