题目内容
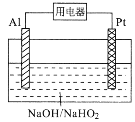
【题目】某碱性电池的总反应为:3HO2-+2Al=OH-+2AlO2-+H2O,工作原理如图所示。下列叙述错误的是
A.电子迁移方向:Al→用电器→Pt
B.电池工作时,负极附近溶液pH减小
C.正极反应式为:HO2-+3H+ +2e-=2H2O
D.负极会发生副反应:2Al+2OH-+2H2O=2AlO2-+3H2↑
【答案】C
【解析】
根据电池总反应3HO2-+2Al=OH―+2AlO2-+H2O,可知Al为电池的负极,电极反应为![]() ,HO2-为正极,电极反应为
,HO2-为正极,电极反应为![]() 。
。
A. 由于Al为电池负极,电子迁移方向:Al→用电器→Pt,A正确;
B. 根据电池的负极反应![]() ,电池工作时,负极附近溶液pH减小,B正确;
,电池工作时,负极附近溶液pH减小,B正确;
C. 因为电池的电解液为碱性环境,故正极的反应式应为![]() ,C错误;
,C错误;
D. 由于负极的Al会直接与碱液接触,故负极会发生副反应:2Al+2OH-+2H2O=2AlO2-+3H2↑,D正确;
故答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
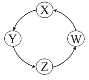
【题目】下列各组物质中,满足表中图示物质在一定条件下,一步转化关系的组合有( )
序号 | X | Y | Z | W |
|
① | Si | Na2SiO3 | H2SiO3 | SiO2 | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A.①②③B.①③C.②③D.①④