题目内容
19.X、Y、Z、L、M五种元素的原子序数依次增大,X的阴离子与Y的内层电子数相等,Y原子的最外层电子数是次外层电子数的两倍,Z、L是空气中含量最多的二种元素,M是地壳中含量最高的金属元素.回答下列问题:(1)X与L形成的常见阴离子的电子式为
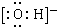 .
.(2)Z、X两元素按原子数目比1:3和2:4构成分子A和B,用电子式表示A的形成过程3H•+
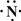 →
→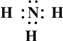 ,B的结构式
,B的结构式
(3)硒是人体必须的微量元素,与L同一主族,硒原子比L原子多两个电子层,则硒在周期表的位置为第四周期第ⅥA族,其最高价氧化物水化物的化学式为H2SeO4.
分析 X、Y、Z、L、M五种元素的原子序数依次增大,Z、L是空气中含量最多的二种元素,则Z为N元素,L为O元素;M是地壳中含量最高的金属元素,则M为Al元素;Y原子的最外层电子数是次外层电子数的两倍,Y有2个电子层,最外层电子数为4,故Y为C元素;X的阴离子与Y的内层电子数相等,X的阴离子有2个电子,故X为H元素.
解答 解:X、Y、Z、L、M五种元素的原子序数依次增大,Z、L是空气中含量最多的二种元素,则Z为N元素,L为O元素;M是地壳中含量最高的金属元素,则M为Al元素;Y原子的最外层电子数是次外层电子数的两倍,Y有2个电子层,最外层电子数为4,故Y为C元素;X的阴离子与Y的内层电子数相等,X的阴离子有2个电子,故X为H元素.
(1)H元素与O元素形成的常见阴离子为OH-,电子式为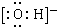 ,故答案为:
,故答案为: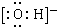 ;
;
(2)Z为N元素、X为H元素,两元素按原子数目比1:3和2:4构成分子A为NH3,B为N2H4,用电子式表示NH3的形成过程为:3H•+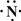 →
→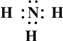 ,N2H4的结构式为
,N2H4的结构式为 ,
,
故答案为:3H•+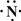 →
→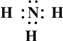 ;
; ;
;
(3)硒(Se)与O元素同一主族,硒原子比L原子多两个电子层,则硒在周期表的位置为:第四周期第ⅥA族,最高化合价为+6价,最高价氧化物对应的水化物化学式为H2SeO4;
故答案为:第四周期第ⅥA族;H2SeO4.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,注意掌握电子式表示物质或化学键的形成,难度不大.

练习册系列答案
相关题目
9.x、y为两元素的原子,x的阴离子与y的阳离子的电子层结构相同,由此可知( )
| A. | x的原子半径大于y的原子半径 | |
| B. | x的第一电离能小于y 的第一电离能 | |
| C. | x的金属性大于y的金属性 | |
| D. | x的电负性大于y的电负性 |
14.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 澄清透明的溶液中:K+、SO42-、Cu2+、Cl- | |
| B. | 0.1mol/L 的FeCl2的溶液中:H+、Na+、NO3-、Cl- | |
| C. | 使甲基橙变红的溶液中:K+、HCO3-、Ba2+、I- | |
| D. | c(H+)/c(OH-)=1×10-12:NH4+、Cl-、Ca2+、Br- |
4.下列说法正确的是( )
| A. | 乙烯分子与苯分子中碳碳键不同,但二者都能发生加成反应 | |
| B. | 苯及其同系物均不能使溴水和酸性高锰酸钾溶液褪色 | |
| C. | 苯的二氯代物有3种,说明苯分子是由6个碳原子以单双键交替结合而成的六元环结构 | |
| D. | 乙酸和乙醇在浓硫酸作用下可以反应,该反应属于加成反应 |
11.现有5种基团:-CH3、-OH、-CHO、-COOH、-C6H5,对由其中两两基团构成且显酸性的有关物质叙述正确的是( )
| A. | 共有4种,其中一种物质不属于羧酸 | |
| B. | 共有5种,其中一种为二元酸 | |
| C. | 共有6种,其中只有一种不是有机酸 | |
| D. | 共有6种,它们在一定条件下均能与乙醇发生酯化反应 |
1.某温度下,碳和H2O(g)在密闭容器里发生下列反应:①C(s)+H2O(g)?CO(g)+H2(g),②CO(g)+H2O(g)?CO2(g)+H2(g)当反应达到平衡时,c(H2)=1.9mol•L-1、c(CO)=0.1mol•L-1.则下列叙述正确的是( )
| A. | CO在平衡时转化率为10% | |
| B. | 平衡浓度c(CO2)=c(H2) | |
| C. | 其他条件不变时,缩小体积,反应②平衡不移动 | |
| D. | 平衡时增大碳的质量,反应①中热量值不变 |
2.冶炼金属的方法有多种,冶炼铝选用的方法是( )
| A. | 铝热法 | B. | 电解法 | C. | 热还原法 | D. | 热分解法 |