题目内容
7.A、B、D、E是周期表中前20号元素,它们的原子序数依次增大.EA2与水反应产生可燃性气体和白色浆状物,向该浆状物中通入AB2气体可得另一白色不溶物.B、D同主族,D的阴离子与E的阳离子具有相同的核外电子排布.请回答:(1)写出元素符号:AC、BO.
(2)镁条在AB2中燃烧的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
(3)将D单质放入浓HNO3中加热,生成红棕色气体和一种强酸,该反应的离子方程式为S+4H++6NO3-$\frac{\underline{\;\;△\;\;}}{\;}$SO42-+6NO2↑+2H2O.
(4)A可形成二元弱酸H2A2O4,0.1molH2A2O4与100mL 2mol/L的KOH溶液反应后,溶液中的离子浓度由大到小的排列顺序是c(K+)>c(C2O42-)>c(OH-)>c(HC2O4-)>c(H+).
分析 A、B、D、E是周期表中前20号元素,它们的原子序数依次增大.EA2与水反应产生可燃性气体和白色浆状物,向该浆状物中通入AB2气体可得另一白色不溶物,两反应分别为:碳化钙与水反应生成乙炔与氢氧化钙,二氧化碳与氢氧化钙反应生成碳酸钙,可推知A为C、B为O、E为Ca,EA2为CaC2,AB2为CO2.B、D同主族,D的阴离子与E的阳离子具有相同的核外电子排布,则D为S元素,据此解答.
解答 解:A、B、D、E是周期表中前20号元素,它们的原子序数依次增大.EA2与水反应产生可燃性气体和白色浆状物,向该浆状物中通入AB2气体可得另一白色不溶物,两反应分别为:碳化钙与水反应生成乙炔与氢氧化钙,二氧化碳与氢氧化钙反应生成碳酸钙,可推知A为C、B为O、E为Ca,EA2为CaC2,AB2为CO2.B、D同主族,D的阴离子与E的阳离子具有相同的核外电子排布,则D为S元素.
(1)由上述分析可知,A为C元素,B为O元素,故答案为:C;O;
(2)镁条在CO2中燃烧的化学方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
(3)将硫单质放入浓HNO3中加热,生成红棕色气体和一种强酸,反应生成二氧化氮与硫酸,该反应的离子方程式为:S+4H++6NO3-$\frac{\underline{\;\;△\;\;}}{\;}$SO42-+6NO2↑+2H2O,
故答案为:S+4H++6NO3-$\frac{\underline{\;\;△\;\;}}{\;}$SO42-+6NO2↑+2H2O;
(4)A可形成二元弱酸H2C2O4,KOH的物质的量为0.1L×2mol/L=0.2mol,与0.1molH2C2O4恰好反应生成K2C2O4,溶液中C2O42-水解呈碱性,氢氧根离子源于C2O42-水解、水的电离,故溶液中的离子浓度由大到小的排列顺序是:c(K+)>c(C2O42-)>c(OH-)>c(HC2O4-)>c(H+),
故答案为:c(K+)>c(C2O42-)>c(OH-)>c(HC2O4-)>c(H+).
点评 本题考查元素化合物推断,关键是根据反应现象及物质组成进行推断,需要学生熟练掌握元素化合物知识,难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 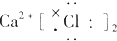 | B. | 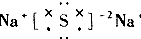 | C. | 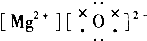 | D. | 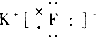 |
| A. | Fe2+、H+、Na+、NO3- | B. | SiO32-、K+、Br-、H+ | ||
| C. | NH4+、Cl-、Mg2+、SO42- | D. | Na+、OH-、NH4+、I- |
| A. | 推广碳捕集和存储技术,逐步实现二氧化碳零排放 | |
| B. | 对工业废水、生活污水净化处理,减少污染物的排放 | |
| C. | 加大铅蓄电池、含汞锌锰干电池的生产,满足消费需求 | |
| D. | 加大清洁能源的开发利用,提高资源的利用率 |
| A. | 标准状况下,22.4L SO3的分子数为1NA | |
| B. | 3.9g Na2O2固体中阴离子的数目为0.1NA | |
| C. | 1mol Cl2与1mol Fe反应,转移的电子数为2NA | |
| D. | 0.1molN2和C18O含有的中子数均为1.4NA |
| A. | SO2→H2SO4→MgSO4→BaSO4 | B. | Si→SiO2→H2SiO3→Na2SiO3 | ||
| C. | Fe→FeCl2→Fe(OH)2→Fe(OH)3 | D. | Na→Na2SO4→NaOH→Na2CO3 |
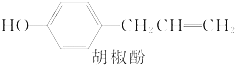
| A. | 该化合物属于芳香烃 | |
| B. | 该化合物的分子式是 C9H11O | |
| C. | 分子中所有碳原子一定处于同一平面 | |
| D. | 1 mol该化合物最多可与4 mol H2发生反应 |
 .
. →
→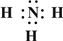 ,B的结构式
,B的结构式