题目内容
【题目】某兴趣小组模拟工业制漂白粉,设计了下列图的实验装置。已知:①氯气和碱反应放出热量。②6Cl2+6Ca(OH)2![]() 5CaCl2+Ca(ClO3)2+6H2O。
5CaCl2+Ca(ClO3)2+6H2O。
回答下列问题:
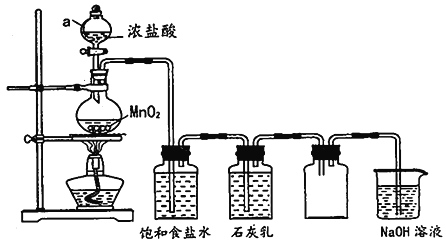
(1)甲装置中仪器a的名称是_____________________。
(2)装置乙中饱和食盐水的作用是_____________________。
(3)①制取漂白粉的化学方程式是______________________________。
②该小组制得的漂白粉中n(CaCl2)远大于n[Ca(ClO)2],则产物中还混杂有物质的化学式是_____。
③为提高Ca(ClO)2的含量,可采取的措施是__________________(任写一种即可)。
(4)漂白粉应密封保存,原因是______________(用化学方程式表示)。
(5)家庭中常用84 消毒液(主要成分NaClO)、洁厕灵(主要成分盐酸)清洁卫生。两者同时混合使用会产生有毒的氯气,写出该反应的离子方程式________________________________。
【答案】分液漏斗除去氯气中混有的氯化氢2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2OCa(ClO3)2将丙装置浸在盛有冷水的水槽中或控制氯气产生速率(其它合理答案也给分)Ca(ClO)2+CO2+H2O=CaCO3↓+2HClOClO-+Cl-+2H+=Cl2↑+H2O
【解析】
(1)甲装置中仪器a具有球形特征,有玻璃活塞,在该实验中,可以控制加入的浓盐酸,为分液漏斗。
(2)浓盐酸和二氧化锰反应过程中会挥发出氯化氢气体,氯化氢在氯化钠饱和溶液中易溶,而氯气难溶,因此饱和食盐水的作用是除去Cl2中混有的HCl气体。
(3)①制取漂白粉的化学方程式是2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。
②氯气和碱反应会放出热量,导致温度升高,当温度低时,氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水;当温度高时,发生了副反应:6Cl2+6Ca(OH)2![]() 5CaCl2+Ca(ClO3)2+6H2O,所以制得的漂白粉中n(CaCl2)远大于n[Ca(ClO)2],即还混有的杂质物质的化学式是Ca(ClO3)2。③温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可以将丙装置浸在盛有冷水的水槽中,或控制氯气产生速率,通过控制反应速率,避免反应放热瞬时温度升高。
5CaCl2+Ca(ClO3)2+6H2O,所以制得的漂白粉中n(CaCl2)远大于n[Ca(ClO)2],即还混有的杂质物质的化学式是Ca(ClO3)2。③温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可以将丙装置浸在盛有冷水的水槽中,或控制氯气产生速率,通过控制反应速率,避免反应放热瞬时温度升高。
(4)漂白粉有效成分为次氯酸钙,HClO虽然具有强氧化性,但它是比碳酸还弱的酸,受空气中的水、CO2作用而导致变质,生成CaCO3和HClO,该反应的化学方程式为Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,所以漂白粉应密封保存。
(5)NaClO与盐酸同时混合使用会发生氧化还原反应产生有毒的氯气,该反应的离子方程式为ClO-+Cl-+2H+=Cl2↑+H2O。

 高效智能课时作业系列答案
高效智能课时作业系列答案【题目】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。通过对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
(1)已知:H2的燃烧热为285.8 kJ·mol-1 H2O(g)=H2O(l) ΔH=-44 kJ/mol
N2(g)+2O2(g)=2NO2(g) ΔH=+133 kJ/mol
①在催化剂存在下,H2还原NO2生成水蒸气和另一种无毒物质的热化学方程式为:___________________________________。
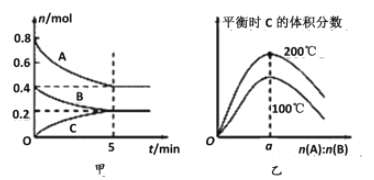
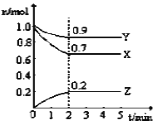
②反应2NO2(g )=N2(g)+2O2(g),设起始时容器中只有NO2,平衡时三种物质的物质的量与温度关系如图所示。
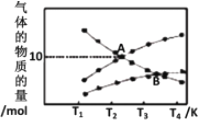
则A点时,NO2的转化率为_______________。
B点时,设容器的总压为a Pa,则平衡常数Kp为____(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)向2 L密闭容器中加入2 mol CO2和6 mol H2,在适当的催化剂作用下,下列反应能自发进行:CO2(g)+3H2(g)![]() CH3OH(g) +H2O(g)。
CH3OH(g) +H2O(g)。
①该反应ΔH_______0(填“>”、“<”或“=”)
②下列叙述能说明此反应达到平衡状态的是____________。(填字母)
a.混合气体的平均相对分子质量保持不变
b.1 mol CO2生成的同时有3 mol H—H键断裂
c.CO2的转化率和H2的转化率相等
d.混合气体的密度保持不变
③反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),在起始温度(T1℃)、体积相同(2L)的两密闭容器中,改变条件,反应过程中部分数据见下表:
CH3OH(g)+H2O(g),在起始温度(T1℃)、体积相同(2L)的两密闭容器中,改变条件,反应过程中部分数据见下表:
反应时间 | CO2/mol | H2/mol | CH3OH/mol | H2O/mol | |
反应Ⅰ:恒温恒容 | 0 min | 2 | 6 | 0 | 0 |
10 min | 4.5 | ||||
20 min | 1 | ||||
30 min | 1 | ||||
反应Ⅱ:绝热恒容 | 0 min | 0 | 0 | 2 | 2 |
反应Ⅰ,前10min内的平均反应速率v(CH3OH)=____________。达到平衡时,反应Ⅰ、Ⅱ对比:平衡常数K(I)____________K(II)(填“>”、“<”或“=”);平衡时CH3OH的浓度c(I)____________c(II)(填“>”、“<”或“=”)。