题目内容
【题目】Ⅰ、(1)惰性电极电解硫酸铜溶液的化学方程式_____________________________。
(2)惰性电极电解饱和食盐水的化学方程式_____________________________。
Ⅱ、某小组同学认为,如果模拟工业上用离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
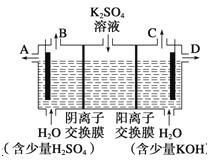
(3)该电解槽的阳极反应式为________________________________。此时通过阴离子交换膜的离子数________(填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数。
(4)制得的氢氧化钾溶液从出口________(填写“A”、“B”、“C”或“D”)导出。
(5)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的反应式为____________________________________________________。
【答案】 2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4 2NaCl+2H2O
2Cu+O2↑+2H2SO4 2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ 4OH--4e-===2H2O+O2↑ 小于 D O2+2H2O+4e-===4OH-
2NaOH+H2↑+Cl2↑ 4OH--4e-===2H2O+O2↑ 小于 D O2+2H2O+4e-===4OH-
【解析】试题分析:Ⅰ、(1)惰性电极电解硫酸铜溶液的生成Cu、O2、H2SO4;(2)惰性电极电解饱和食盐水生成氢氧化钠、氢气、氯气;Ⅱ、(3)阳极OH-失电子发生氧化反应生成氧气;通过阴离子交换膜的离子是SO42-,通过阳离子交换膜的离子是K+;(4)阴极反应生成![]() ,所以氢氧化钾溶液在阴极生成;(5)氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,正极是氧气得电子生成OH-。
,所以氢氧化钾溶液在阴极生成;(5)氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,正极是氧气得电子生成OH-。
解析:Ⅰ、(1)惰性电极电解硫酸铜溶液的生成Cu、O2、H2SO4,总反应是2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4;(2)惰性电极电解饱和食盐水生成氢氧化钠、氢气、氯气,总反应是2NaCl+2H2O
2Cu+O2↑+2H2SO4;(2)惰性电极电解饱和食盐水生成氢氧化钠、氢气、氯气,总反应是2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;Ⅱ、(3)阳极OH-失电子发生氧化反应生成氧气,阳极反应式为4OH--4e-===2H2O+O2↑;通过阴离子交换膜的离子是SO42-,通过阳离子交换膜的离子是K+,根据电荷守恒通过阴离子交换膜的离子数小于通过阳离子交换膜的离子数;(4)阴极反应生成
2NaOH+H2↑+Cl2↑;Ⅱ、(3)阳极OH-失电子发生氧化反应生成氧气,阳极反应式为4OH--4e-===2H2O+O2↑;通过阴离子交换膜的离子是SO42-,通过阳离子交换膜的离子是K+,根据电荷守恒通过阴离子交换膜的离子数小于通过阳离子交换膜的离子数;(4)阴极反应生成![]() ,所以氢氧化钾溶液在阴极生成,制得的氢氧化钾溶液从出口D放出;(5)氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,正极是氧气得电子生成OH-,正极的反应式为O2+2H2O+4e-===4OH-。
,所以氢氧化钾溶液在阴极生成,制得的氢氧化钾溶液从出口D放出;(5)氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,正极是氧气得电子生成OH-,正极的反应式为O2+2H2O+4e-===4OH-。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案