题目内容
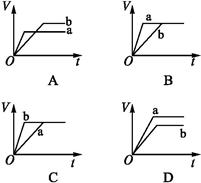
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)=Si(s)+4HCl(g) ΔH=+Q kJ·mol-1(Q>0),某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应(此条件下为可逆反应),下列叙述正确的是( )
| A.反应过程中,若增大压强能提高SiCl4的转化率 |
| B.若反应开始时SiCl4为1 mol,则达到平衡时,吸收热量为Q kJ |
| C.反应至4 min时,若HCl的浓度为0.12 mol·L-1,则H2的反应速率为0.03 mol·L-1·min-1 |
| D.当反应吸收热量为0.025 Q kJ时,生成的HCl通入100 mL 1 mol·L-1的NaOH溶液恰好反应 |
D
解析

练习册系列答案
相关题目
在一定条件下,将3 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g)。2 min末该反应达到平衡,生成 0.8 mol D,并测得C的浓度为0.2 mol·L-1,下列判断正确的是
xC(g)+2D(g)。2 min末该反应达到平衡,生成 0.8 mol D,并测得C的浓度为0.2 mol·L-1,下列判断正确的是
| A.平衡常数约为0.3 |
| B.B的转化率为60% |
| C.A的平均反应速率为0.3 mol/(L·min) |
| D.若混合气体的密度不变则表明该反应达到平衡状态 |
铜锌原电池(如图)工作时,下列叙述正确的是( )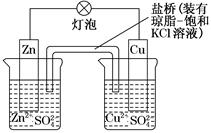
| A.正极反应为:Zn―→Zn2++2e- |
| B.电池反应为:Zn+Cu2+=Zn2++Cu |
| C.在外电路中,电子从正极流向负极 |
| D.盐桥中的K+移向ZnSO4溶液 |
在容积可变的密闭容器中,2 mol N2和8 mol H2在一定条件下发生反应,达到平衡时,H2的转化率为25%,则平衡时氮气的体积分数接近于( )
| A.5% | B.10% | C.15% | D.20% |
下列说法不正确的是( )
| A.焓变是一个反应能否自发进行相关的因素,多数放热反应能自发进行 |
| B.自发进行的反应一定能迅速进行 |
| C.在同一条件下不同物质有不同的熵值,其体系的混乱程度越大,熵值越大 |
| D.一个反应能否自发进行,可用焓变和熵变共同判断 |
高温下,某反应达平衡,平衡常数K=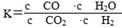 ,恒容时,温度升高,H2浓度减小。下列说法正确的是( )
,恒容时,温度升高,H2浓度减小。下列说法正确的是( )
| A.该反应的焓变为正值 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
D.该反应化学方程式为CO+H2O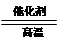 CO2+H2 CO2+H2 |
下列反应中,在高温下不能自发进行的是( )
A.CO(g) C(s)+O2(g) C(s)+O2(g) |
B.NH4Cl(s) NH3(g)↑+HCl(g)↑ NH3(g)↑+HCl(g)↑ |
C.(NH4)2CO3(s) NH4HCO3(s)+NH3(g) NH4HCO3(s)+NH3(g) |
D.MgCO3(s) MgO(s)+CO2(g) MgO(s)+CO2(g) |