题目内容
12.我国已对酒驾实行了“醉驾入刑”,酒的主要成分是乙醇.请回答下列问题:(1)乙醇的官能团是-OH或羟基;
(2)使用K2Cr2O7酸性溶液检测酒驾,利用了乙醇的还原性(填“氧化性”或“还原性”).
分析 乙醇含有羟基,可发生取代、消去和氧化反应,以此解答该题.
解答 解:(1)乙醇含有的官能团为-OH 或羟基,故答案为:-OH 或羟基;
(2)乙醇含有羟基,被K2Cr2O7酸性溶液氧化,表现还原性,故答案为:还原性.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的官能团的性质,难度不大.

练习册系列答案
相关题目
2.常温下,在一定体积某浓度的BaCl2溶液中,逐滴加入pH=1的稀硫酸至溶液中的Ba2+恰好完全沉淀时,测得溶液pH=2.若忽略两溶液混合时的体积变化,则加入稀硫酸的体积与原BaCl2溶液的体积比是( )
| A. | 10:1 | B. | 1:10 | C. | 9:1 | D. | 1:9 |
3.香柠檬酚具有抗氧化功能,它的结构如图,下列说法正确的是( )
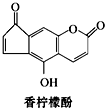

| A. | 它的分子式为C13H9O4 | |
| B. | 它与H2发生加成反应,1 mol最多可消耗7 mol H2 | |
| C. | 它与溴水发生反应,1 mol最多消耗3 mol Br2 | |
| D. | 它与NaOH溶液反应,1 mol最多消耗2 mol NaOH |
20.下列物质属于纯净物的是( )
| A. | 医用酒精 | B. | 蒸馏水 | C. | 漂白粉 | D. | 空气 |
7.下列反应属于吸热反应的是( )
| A. | 甲烷在空气中燃烧 | B. | 碳酸钙受热分解 | ||
| C. | 镁条溶于盐酸 | D. | 过氧化钠与水反应 |
4.可逆反应:A+B?C,在低温下能自发进行,在高温下不能自发进行,对该反应过程△H、△S的判断正确的是( )
| A. | △H>0、△S>0 | B. | △H<0、△S<0 | C. | △H<0、△S>0 | D. | △H>0、△S<0 |
1.下列所描述的二氧化硫的一些化学性质中,体现二氧化硫作为还原剂的是( )
| A. | 通入溴水溶液使溴水褪色 | B. | 通入品红溶液中,使品红褪色 | ||
| C. | 溶于水形成不稳定的亚硫酸 | D. | 与碱液反应生成亚硫酸盐 |