题目内容
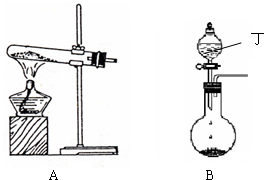
将CO2通入饱和Na2CO3溶液中,会发生
溶液变浑浊(或有晶体析出)
溶液变浑浊(或有晶体析出)
现象,这说明碳酸氢钠的溶解度小于碳酸钠
碳酸氢钠的溶解度小于碳酸钠
,有关反应的化学方程式为Na2CO3+CO2+H2O═2NaHCO3
Na2CO3+CO2+H2O═2NaHCO3
.分析:向饱和的碳酸钠溶液中加入二氧化碳后会生成碳酸氢钠,可以据此来答题.
解答:解:碳酸钠与二氧化碳反应后要生成碳酸氢钠:Na2CO3+CO2+H2O═2NaHCO3↓,而碳酸氢钠的溶解度小于碳酸钠,所以溶液变浑浊(或有晶体析出).
故答案为:溶液变浑浊(或有晶体析出);碳酸氢钠的溶解度小于碳酸钠;Na2CO3+CO2+H2O═2NaHCO3.
故答案为:溶液变浑浊(或有晶体析出);碳酸氢钠的溶解度小于碳酸钠;Na2CO3+CO2+H2O═2NaHCO3.
点评:书写化学方程式时,首先分析应用的原理,然后根据反应物、生成物书写方程式,注意要遵守书写规则.

练习册系列答案
相关题目
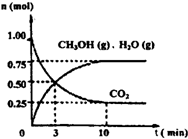 (2012?信阳二模)如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究.
(2012?信阳二模)如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究.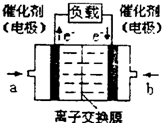

 +CO2+H2O→
+CO2+H2O→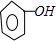 +NaHCO3;
+NaHCO3;