题目内容
9.下列叙述中正确的是( )| A. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照条件下和点燃条件下的△H不同 | |
| B. | 常温下反应2A(s)+B(g)═2C(g)+D(g)不能自发进行,则反应的焓变一定大于零 | |
| C. | 需要加热的化学反应,生成物的总能量一定高于反应物的总能量 | |
| D. | 等质量的硫粉分别在空气、氧气中燃烧,放出热量多的是硫粉在氧气燃烧 |
分析 A.反应的热效应只与始态、终态有关,与过程无关;
B.反应自发进行的判断依据是△H-T△S<0;
C.生成物的总能量低于反应总能量的反应,是放热反应,若是吸热反应则相反,与反应条件无关;
D.反应热只与反应物的量及其状态有关.
解答 解:A.反应的热效应只与始态、终态有关,与过程无关,所以同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H相同,故A错误;
B.反应自发进行的判断依据是△H-T△S<0自发,△H-T△S>0不自发,已知常温下,反应2A(s)+B(g)=2C(g)+D(g)为熵增大的反应即△S>0,若△H-T△S>0,则反应的焓变一定大于零,故B正确;
C.生成物的总能量低于反应总能量的反应,是放热反应,若是吸热反应则相反,与反应条件无关,所以需要加热的化学反应,不一定是生成物的总能量高于反应物的总能量,故C错误;
D.反应热只与反应物的量及其状态有关,所以等质量的硫粉分别在空气、氧气中燃烧,放出热量一样多,故D错误;
故选B.
点评 本题考查化学变化特征、反应自发性的判断、能量转化形式等,比较基础,注意对基础知识的理解掌握.

练习册系列答案
相关题目
20.在一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应A(s)+2B(g)?C(g)+D(g)已达到平衡状态的是( )
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度
④气体总物质的量 ⑤混合气体的平均相对分子质量 ⑥v(C)与v(D)的比值.
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度
④气体总物质的量 ⑤混合气体的平均相对分子质量 ⑥v(C)与v(D)的比值.
| A. | ②③⑤ | B. | ①②③ | C. | ②③④⑥ | D. | ①③④⑤ |
17.磷酸铁锂(LiFePO4)电池是可循环使用的二次电池,其循环寿命是铅蓄电池的4-7倍,并有大容量、无记忆效应等优点,可用于电动汽车.该电池的正极材料是LiFePO4,负极材料是锂,电池反应为:LiFePO4$?_{放电}^{充电}$ FePO4+Li,使用含Li+导电固体为电解质.下列有关LiFePO4电池说法正确的是( )
| A. | 可加入硫酸、氢氧化钾等强电解质以提高电解质的导电性 | |
| B. | 放电时电池内部Li+向负极移动 | |
| C. | 放电过程中,电池正极材料的质量不变 | |
| D. | 放电时电池正极反应为:FePO4+Li++e-═LiFePO4 |
4.物质的量之比为1:3的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,下列说法正确的是( )
| A. | 在此反应中硝酸体现强氧化性,全部被还原 | |
| B. | 向反应后的溶液中再加入金属铁,不再发生化学反应 | |
| C. | 原混合物在反应后,被还原的硝酸与未被还原的硝酸之比为1:4 | |
| D. | 原混合物在反应后,被还原的硝酸与未被还原的硝酸之比为1:5 |
1.下列物质暴露于空气中,其质量改变和空气中的成分没有关系的是( )
| A. | 生石灰 | B. | 铁粉 | C. | 浓硫酸 | D. | 浓盐酸 |
18.将少量的CO2通入下列溶液中,不能产生沉淀的是( )
| A. | 硅酸钠溶液 | B. | 偏铝酸钠溶液 | C. | 氢氧化钡溶液 | D. | 氯化钙溶液 |
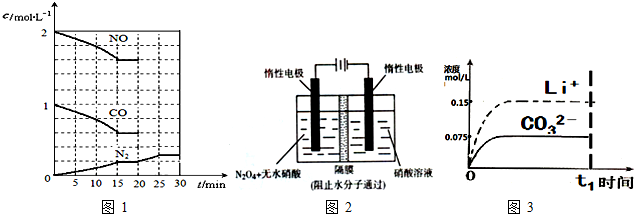 (填“向左”、“向右”或“不”).
(填“向左”、“向右”或“不”).
 ;
; 化学中有许多有趣的实验,如下介绍的“蓝瓶子”实验就是一例.在250mL圆底烧瓶中依次加入2g氢氧化钠、100mL蒸馏水、2g葡萄糖(粉末),振荡使其溶解.滴入4〜6滴0.2%的亚甲基蓝溶液,塞上瓶塞(如图):
化学中有许多有趣的实验,如下介绍的“蓝瓶子”实验就是一例.在250mL圆底烧瓶中依次加入2g氢氧化钠、100mL蒸馏水、2g葡萄糖(粉末),振荡使其溶解.滴入4〜6滴0.2%的亚甲基蓝溶液,塞上瓶塞(如图):