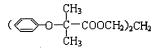
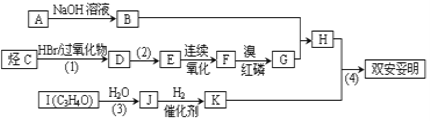
题目内容
【题目】氨是重要的化工原料,用途广泛。
(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+和CH3COO-构成)溶液吸收对氨合成催化剂(铁粉)有毒害的CO气体。
①醋酸二氨合铜所含的元素中,第一电离能最大的是 。(填元素符号)
②醋酸二氨合铜所含元素的单质,所属的晶体类型有 (填序号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期中,基态原子与基态Cu原子未成对电子数目相同的元素有 种(不包括Cu)。
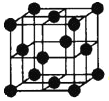
④铜单质为面心立方晶体,其晶胞如图。如果Cu的原子半径为a cm,阿伏加德常数的值为NA,则此种Cu单质的密度表达式为 g/cm3。(相对原子质量Cu:64)

(2)BF3气体与NH3相遇立即生成一种白色晶体:BF3+ NH3=F3B—NH3。写出两种与BF3具有相同空间构型的阴离子 、 。
(3)NH3可用于合成尿素、硫酸铵等氮肥。某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质。该物质在水溶液中以SO42-和N4H44+两种正四面体构型的离子存在。N4H44+遇碱生成一种形似白磷的N4分子。画出N4H44+的结构(标明其中的配位键) 。
【答案】(1)① 氮 ② b、c、d③ 4④![]() (2) CO32-、NO3-(3)
(2) CO32-、NO3-(3)
【解析】
试题分析:(1)①非金属性越强,第一电离能越大,但是最外层电子排布处于全满或半满状态时较稳定,不易失电子,第一电离能较大,醋酸二氨合铜所含的元素有Cu、O、C、H、N,由于N原子的最外层排布为半满状态,第一电离能较大,所以第一电离能最大的是氮;
②醋酸二氨合铜所含元素组成的单质,铜属于金属晶体、金刚石属于原子晶体、氧气和氢气属于分子晶体,答案选b、c、d;
③Cu的外围电子排布为3d104s1,只有1个未成对电子,第4周期元素中,基态原子含有一个未成对电子的元素有,K、Sc、Ga、Br,共有4种元素;
④该晶胞中铜原子个数=8×1/8+6×1/2=4,晶胞边长为acm,晶胞体积=(acm)3,密度ρ=(4×M/NA)/V=![]() ;
;
(2)BF3中B的价层电子对数为3+(3-3×1)/2=3,没有孤电子对,分子的空间构型为正三角形,CO32-中碳原子价层电子对个数=3+(4+2-3×2)×1/2=3,且不含孤电子对,所以C原子采用sp2杂化,空间构型为平面三角形,NO3-中N原子形成3个σ键,孤对电子数=(5+13×2)/2,中心原子为sp2杂化,立体构型为平面三角形,所以与BF3具有相同空间构型的阴离子为CO32-;NO3-;
(3)N4H44+中每个N原子与另外3个N原子形成共价键,同时与1个氢离子形成配位键,则N4H44+的结构为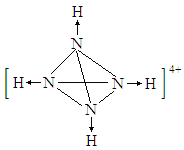 。
。

【题目】类比法是一种重要的化学思维方法。下列各项中的已知和类比结论均正确的是
选项 | 已知 | 类比结论 |
A | 汞可以用热分解法冶炼 | 铜也可以用热分解法冶炼 |
B | Mg-Al插入稀H2SO4溶液中构成 原电池,Mg作负极 | Mg-Al插入稀NaOH溶液中构成原电池,Mg也作负极 |
C | 硫元素的最高正化合价为+6 | 氧元素的最高正化合价也为+6 |
D | Si是半导体材料 | Ge也可作半导体材料 |
A.AB.BC.CD.D