题目内容
18.下列关于实验现象解释不正确的是( )| A | B | C | D | |
| 操作与现象 | 放在石棉网上的钠在空气中燃烧生成黑色固体 | 铜与稀硝酸反应试管内产生红棕色气体 | 0.5mol/L的CaCl2滴入0.5mol/L的NaHCO3中产生白色沉淀 | Cu与浓硫酸反应生成白色及少量黑色沉淀物 |
| 解释 | 生成固体物质有大量的碳 | 反应产生的NO与试管内的空气反应 | 反应2HCO3-+Ca2+=CaCO3↓+H2O+CO2↑ | 白色沉淀是CuSO4黑色沉淀是Cu2O |
| A. | A | B. | B | C. | C | D. | D |
分析 A.钠在空气中燃烧产物是淡黄色的过氧化钠;
B.铜与稀硝酸反应生成NO,在试管口转化为NO2;
C.0.5mol/L的CaCl2滴入0.5mol/L的NaHCO3中产生白色沉淀,是由于碳酸氢根离子电离出的碳酸根离子和钙离子的乘积大于其碳酸钙的溶度积;
D.浓硫酸与铜片共热时,白色沉淀是CuSO4,同时有黑色沉淀物CuS.
解答 解:A.将金属钠放在石棉网上用酒精灯加热后,金属钠剧烈燃烧,产生黄色火焰,生成淡黄色固体过氧化钠,故A错误;
B.铜与稀硝酸反应3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O,反应产生的NO与试管内的空气反应2NO+O2=2NO2,试管内产生红棕色NO2气体,故B正确;
C.0.5mol/L的CaCl2滴入0.5mol/L的NaHCO3中,碳酸氢根离子电离出的碳酸根离子和钙离子的乘积大于其碳酸钙的溶度积,发生反应:2HCO3-+Ca2+=CaCO3↓+H2O+CO2↑,故C正确;
D.Cu与浓H2SO4的主反应为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2+2H2O,由于浓H2SO4过量且浓硫酸具有吸水性,故所得白色固体为CuSO4;Cu与浓硫酸反应生成少量黑色沉淀物4Cu+4H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$3CuSO4+CuS↓+4H2O,黑色沉淀是CuS,故D错误;
故选AD.
点评 本题考查元素化合物知识,题目难度中等,根据反应实验现象进行分析,B选项注意铜与稀硝酸的性质角度思考.

练习册系列答案
相关题目
8.下列解释事实的方程式正确的是( )
| A. | 利用铝热反应焊接钢轨:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$ 2Fe+Al2O3 | |
| B. | 用氯水除去FeCl3溶液中的Fe2+:Cl2+Fe2+═2Cl-+Fe3+ | |
| C. | 用已知浓度的NaOH溶液测定未知浓度的醋酸溶液的浓度:H++OH-═H2O | |
| D. | 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2Na++2OH-═Na2SiO3+H2O |
9.下列关于25℃的NaHCO3溶液的相关事实,能够证明H2CO3为弱酸的是( )
| A. | 溶液中存在CO32- | B. | 溶液中c(Na+)>c(CO32-) | ||
| C. | 与等物质的量的NaOH恰好中和 | D. | 溶液中c(H+)•c(OH-)=10-14 |
6.表中的W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法正确的是( )
| X | Y | ||
| W | Z |
| A. | 最高价氧化物对应水化物的酸性:Z>X>W | |
| B. | 最低价氢化物的沸点:Z>Y>X | |
| C. | 原子半径:W>X>Y>Z | |
| D. | 由X、Y和氢三种元素只能形成含有共价键的化合物 |
13.下列说法正确的是( )
| A. | CH2O2和C3H6O2一定互为同系物 | |
| B. | 碳酸钠溶液可用于鉴别乙酸和乙酸乙酯 | |
| C. | 用溴水可以除去溶解在苯中的少量苯酚 | |
| D. | 粮食酿酒过程中,淀粉在酶的催化作用下最终水解为乙醇 |
3.用下列实验装置进行的实验中,不能达到相应实验目的是( )
| A. | 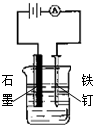 装置:防止铁钉生锈 | B. |  装置:可制得金属锰 | ||
| C. |  装置:实验室制取乙酸乙酯 | D. | 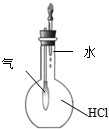 装置:验证HCl气体在水中的溶解性 |
10.化学与生活密切相关,下列说法正确的是( )
| A. | 使用漂白液时不可与酸性洁厕剂混用 | |
| B. | 淘米水中含有淀粉可以直接检测加碘盐中是否含有碘元素 | |
| C. | 葡萄糖、油脂、蛋白质等进入人体内经水解后被吸收 | |
| D. | 铝壶表面有致密氧化膜耐腐蚀,可长期存放食醋 |
5.下列反应中,可以使碳链增长的是( )
| A. | 1溴丙烷与NaOH的醇溶液共热 | B. | 乙醛与H2加成 | ||
| C. | 乙醇与浓H2SO4共热到140℃ | D. | 1-溴丙烷与NaOH的水溶液共热 |
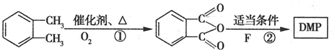
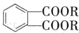 (代号DMP)是一种常用的酯类塑化剂,其相对分子质量为194.工业上生产DMP的流程如图所示:
(代号DMP)是一种常用的酯类塑化剂,其相对分子质量为194.工业上生产DMP的流程如图所示: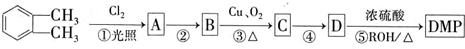
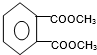 .
. .
.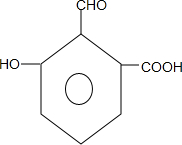 .
.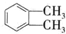 制备DMP的另一种途径:
制备DMP的另一种途径: