题目内容
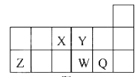
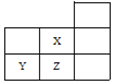
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是( )
A.元素X与元素Z的最高正化合价之和的数值等于8
B.原子半径的大小顺序为:r(X)>r(Y)>r(Z)>r(W)>r(Q)
C.元素W的最高价氧化物对应的水化物的酸性比Q的强
D.离子Y2-和Z3+的核外电子数和电子层数都不相同
【答案】A
【解析】
由图可知,X、Y为第二周期元素,Z、W、Q为第三周期元素,由元素在周期表中相对位置,可知X为N元素,Y为O元素,Z为Al元素,W为S元素,Q为Cl元素,据此分析解答。
A.元素X的最高正价为+5价,元素Z的最高正价为+3价,二者最高正化合价之和的数值等于8,A项正确;
B.根据同周期元素的原子半径随核电荷数的增大而减小,可知原子半径:r(X)>r(Y)、r(Z)>r(W)>r(Q)。根据原子电子层数越多,原子半径越大,可知原子半径大小:r (Z)>r(W)>r(Q)>r(X)>r(Y),B项错误;
C.根据同一周期从左至右非金属性逐渐增强,可知非金属性:Q>W,则最高价氧化物对应水化物的酸性:Q>W,C项错误;
D.离子Y2-为O2-,其核外电子数为10,有2个电子层;Z3+为Al3+,核外电子数为10,有2个电子层,二者的核外电子数和电子层数都相同,D项错误;
答案选A。

练习册系列答案
相关题目
【题目】如图是元素周期表的一部分:
数据编号 | 滴入NaOH溶液的体积 | 溶液的pH | |
HX | HZ | ||
1 | 0 | 3 | 1 |
2 |
| a | b |
![]() 时,用浓度为
时,用浓度为![]() 的氢氧化钠溶液分别滴定
的氢氧化钠溶液分别滴定![]() 浓度均为
浓度均为![]() 的两种酸HX、
的两种酸HX、![]() 忽略体积变化
忽略体积变化![]() ,实验数据如表2,下列判断正确的是
,实验数据如表2,下列判断正确的是![]()
A.通过分析可得表格中![]() ,
,![]()
B.将上述的HZ溶液稀释100倍后pH比HX溶液的pH大
C.由于Z元素的非金属性比Y强,所以Z氢化物的酸性较强
D.![]()
![]()
![]() 的水溶液中:
的水溶液中:![]()
![]()