题目内容
【题目】
钴、铁、镓、砷的单质及其化合物在生产生活中有重要的应用。回答下列问题:
(1) 写出As的基态原子的电子排布式_________________。
(2)N、P、As为同一主族元素,其电负性由大到小的顺序为____________________,它们的氢化物沸点最高的是____________。将NaNO3和Na2O在一定条件下反应得到一种白色晶体,已知其中阴离子与SO42-互为等电子体,则该阴离子的化学式是_____________。
(3) Fe3+、Co3+与N3-、CN-等可形成络合离子。
①K3[Fe(CN)6]可用于检验Fe2+,配体CN-中碳原子杂化轨道类型为______________。
②[Co(N3)(NH3)5]SO4中Co的配位数为____________,其配离子中含有的化学键类型为_______(填离子键、共价键、配位键),C、N、O 的第一电离能最大的为_______,其原因是_____________________。
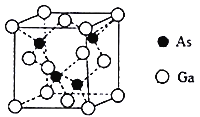
(4) 砷化镓晶胞结构如下图。晶胞中Ga与周围等距且最近的As形成的空间构型为________。已知砷化镓晶胞边长为apm,其密度为pg·cm-3,则阿伏加德罗常数的数值为__________________(列出计算式即可)。
【答案】[Ar] 3d104s24p3 N>P>As NH3 NO43- sp 6 共价键、配位键 N 氮原子2p轨道上的电子为半充满,相对稳定,更不易失去电子 正四面体 ![]()
【解析】
(1)As的原子序数为33,由构造原理可知电子排布为[Ar] 3d104s24p3;(2)As、P、N元素属于同一主族元素,其原子序数逐渐减小,则其电负性逐渐增大,即N>P>As;它们的氢化物中NH3中存在氢键,沸点最高;原子个数相等价电子数相等的微粒属于等电子体,且等电子体结构相似,阴离子与SO42-互为等电子体,且该阴离子中的各原子的最外层电子都满足8电子稳定结构,则该离子是NO43-,(3)① CN-中C原子价层电子对个数=1+![]() (4+1-1×3)=2,所以采取sp杂化;②配位环境是[Co(N3)(NH3)5]SO4,其中N3(-),NH3都是单齿配体,简单相加就得到配位数6;其配离子中含有的化学键类型为共价键、配位键;C、N、O属于同一周期元素且原子序数依次减小,同一周期元素的第一电离能随着原子序数的增大而增大,但氮原子2p轨道上的电子为半充满,相对稳定,更不易失去电子,第ⅤA族的大于第ⅥA族的,所以其第一电离能大小顺序是N>O>C;(4)Ga原子处于晶胞的顶点和面心,面心到顶点和到相邻面心的距离最小且相等,根据图可知
(4+1-1×3)=2,所以采取sp杂化;②配位环境是[Co(N3)(NH3)5]SO4,其中N3(-),NH3都是单齿配体,简单相加就得到配位数6;其配离子中含有的化学键类型为共价键、配位键;C、N、O属于同一周期元素且原子序数依次减小,同一周期元素的第一电离能随着原子序数的增大而增大,但氮原子2p轨道上的电子为半充满,相对稳定,更不易失去电子,第ⅤA族的大于第ⅥA族的,所以其第一电离能大小顺序是N>O>C;(4)Ga原子处于晶胞的顶点和面心,面心到顶点和到相邻面心的距离最小且相等,根据图可知![]() 个,Ga与周围等距离且最近的As形成的空间构型为Ga在中心As在四个顶点形成的正四面体结构;GaAs为1:1型结构,一个晶胞占有4个Ga原子和4个As原子,若晶胞的边长为apm,则晶胞体积为
个,Ga与周围等距离且最近的As形成的空间构型为Ga在中心As在四个顶点形成的正四面体结构;GaAs为1:1型结构,一个晶胞占有4个Ga原子和4个As原子,若晶胞的边长为apm,则晶胞体积为![]() ,晶体的密度为pg·cm-3,则晶胞质量为
,晶体的密度为pg·cm-3,则晶胞质量为![]() pg·cm-3=
pg·cm-3=![]() ,则
,则![]() ,则
,则![]() 。
。

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案【题目】利用右图所示装置进行下列实验,能得出相应实验结论的是( )
选项 | ① | ② | ③ | 实验结论 | 实验装置 |
A | 稀硫酸 | Na2S | AgNO3与AgCl的溶液 | Ksp(AgCl)>Ksp(Ag2S) |
|
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2与可溶性钡盐均可以生成白色沉淀 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
A. A B. B C. C D. D
【题目】POCl3常用作半导体掺杂剂及光导纤维原料,实验室制备POCl3并测定产品含量的实验过程如下:
I.实验室制备POCl3。采用氧气氧化液态PCl3法制取POCl3,实验装置(加热及夹持仪器略)如图:

资料:①Ag++SCN-=AgSCN↓:Ksp(AgCl)>Ksp(Ag SCN);
②PCl3和POCl3的相关信息如下表:
物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
PCl3 | -112.0 | 76.0 | 137.5 | 两者互溶,均为无色液体,遇水均剧烈反应生成含氧酸和氯化氢 |
POCl3 | 2.0 | 106.0 | 153.5 |
(1) 装置B中的作用是观察氧气的流速和______________、_______________ ,干燥管的作用是_____________
(2)反应温度要控制在60~65℃,原因是:________________________________________________
II.测定POCl3产品的含量。
实验步骤:
①制备POCl3实验结束后,待三颈瓶中的液体冷却至室温,准确称取30.7 g产品(杂质不含氯元素),置于盛有60.00 mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00 mL 溶液。
②取10.00 mL溶液于锥形瓶中,加入10.00 mL 3.2 moI/L AgNO3标准溶液。
③加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖。
④以X为指示剂,用0.2 moI/L KSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00 mL KSCN溶液。
(3)实验室用5.0 moI/L AgNO3 配制100 mL 3.2 moI/L AgNO3标准溶液,所使用的仪器除烧杯和玻璃棒外还有_____________________
(4)步骤③若不加入硝基苯的将导致测量结果_____(填偏高、偏低或无影响)
(5)步骤④中X可以选择_____。
(6)反应中POCl3的质量百分含量为_____,通过_____(填操作)可以提高产品的纯度。