题目内容
【题目】下列关于CH4和CO2的说法不正确的是
A. 固态CO2属于分子晶体,其晶体中每个CO2分子周围有12个分子紧邻
B. CH4、CO2分子中均含有极性共价键,均是非极性分子
C. 因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
D. CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
【答案】C
【解析】
A、固态CO2属于分子晶体,晶体构型为: ,由其结构可知,晶体中每个CO2分子周围有12个分子紧邻,故A正确;
,由其结构可知,晶体中每个CO2分子周围有12个分子紧邻,故A正确;
B、CH4分子是正四面体结构,分子结构对称,正负电荷中心的分子为非极性分子,CO2分子为直线型结构,分子结构对称,正负电荷中心的分子为非极性分子,故B正确;
C、分子晶体的熔沸点与分子间作用力有关,CH4的分子间作用力小于CO2,所以CH4熔点低于CO2,与共价键无关,故C错误;
D、CH4中C原子的价层电子对数为4,没有孤电子对,C原子的杂化类型是sp3,CO2分子中碳原子的价层电子对数为2,则其C原子的杂化类是sp,所以CH4和CO2分子中碳原子的杂化类型分别是sp3和sp,故D正确。
综上所述,本题应选C。

【题目】已知反应X(g)+Y(g)![]() R(g)+Q(g)的平衡常数与温度的关系如表所示。830 ℃时,向一个2 L的密闭容器中充入0.2 mol X和0.8 mol Y,反应初始4 s内v(X)=0.005 mol/(L·s)。下列说法正确的是
R(g)+Q(g)的平衡常数与温度的关系如表所示。830 ℃时,向一个2 L的密闭容器中充入0.2 mol X和0.8 mol Y,反应初始4 s内v(X)=0.005 mol/(L·s)。下列说法正确的是
温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
A. 4 s时容器内c(Y)=0.76 mol/L
B. 830 ℃达平衡时,X的转化率为80%
C. 反应达平衡后,升高温度,平衡正向移动
D. 1 200 ℃时反应R(g)+Q(g) ![]() X(g)+Y(g)的平衡常数K=0.4
X(g)+Y(g)的平衡常数K=0.4
【题目】从某含Br—废水中提取Br2的过程包括:过滤、氧化、萃取(需选择合适萃取剂)及蒸馏等步骤。已知:
物质 | Br2 | CCl4 | 正十二烷 |
密度/g·cm-3 | 3.119 | 1.595 | 0.753 |
沸点/℃ | 58.76 | 76.8 | 215~217 |
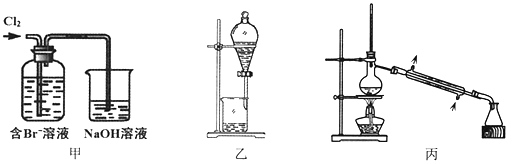
下列说法不正确的是
A. 甲装置中Br—发生的反应为:2Br-+ Cl2 = Br2 + 2Cl-
B. 甲装置中NaOH溶液每吸收0.1mol Cl2,转移0.1mol e—
C. 用乙装置进行萃取,溶解Br2的有机层在下层
D. 用丙装置进行蒸馏,先收集到的是Br2