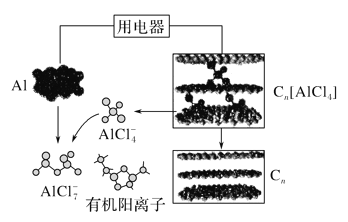
��Ŀ����
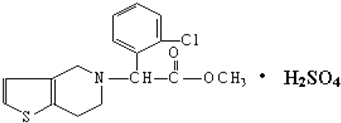
����Ŀ������������Ҫ��ҽҩ��Ⱦ���м��壬��Ӧ�÷dz��㷺��������Ľṹ��ʽ��ͼ��ʾ��
��ش�
��1������������к��������ŵ������� ��
��2��������ķ���ʽ�� ��
��3����������һ�������·����������۷�Ӧ���ɾۺ���Ļ�ѧ����ʽ��
��4���������ж���ͬ���칹�壬��д������һ����������������ͬ���칹��Ľṹ��ʽ�� ��
�ٺ��������ܷ���������Ӧ
���ǻ�ֱ�����ڱ�����
�۱�����ֻ��2��ȡ������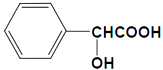
���𰸡�
��1���ǻ����Ȼ�
��2��C8H8O3
��3��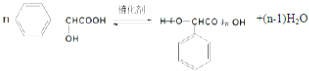
��4��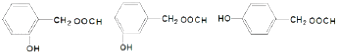
���������⣺��1.�� ![]() �к���OH����COOH��������Ϊ�ǻ����Ȼ������Դ��ǣ��ǻ����Ȼ���
�к���OH����COOH��������Ϊ�ǻ����Ȼ������Դ��ǣ��ǻ����Ȼ���
��2.�����ݽṹ��ʽ ![]() ����֪����ʽΪC8H8O3 �� ���Դ��ǣ�C8H8O3��
����֪����ʽΪC8H8O3 �� ���Դ��ǣ�C8H8O3��
��3.���ǻ������Ȼ�����������Ӧ����ѧ����ʽ 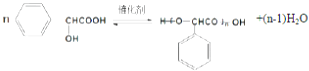 ��
��
���Դ��ǣ�  ��
��
��4.���ܷ���������Ӧ˵������ȩ������Ϣٺ��������ܷ���������Ӧ�����ǻ�ֱ�����ڱ����ϣ��۱�����ֻ��2��ȡ��������֪ͬ���칹��Ϊ�� 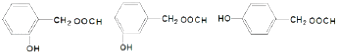 �����Դ��ǣ�
�����Դ��ǣ� 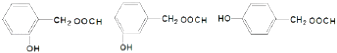 ��
��

 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�����Ŀ���������ʷ������ȷ�����(����)
ѡ�� | �� | �� | �� | ���������� |
A | ���� | ���� | ���� | �������� |
B | �ռ� | ���� | ʳ�� | һ����̼ |
C | ������ | ���� | ʯ��ʯ | ˮ |
D | ������ | ̼�� | ̼��þ | �������� |
A.AB.BC.CD.D