题目内容
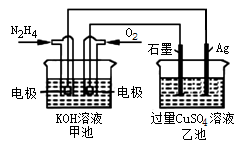
某同学设计了如下图所示的装置进行电化学实验,请你根据装置图回答相关问题:
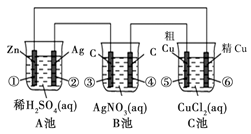
(1)C池属于什么装置 。
(2)电极②上发生电极反应式为 ;B池中发生的总反应方程式为 。
(3)反应进行一段时间后,A、B、C三池中电解质溶液浓度基本不变的是________。
(4)当电路上有0.2 mol电子流过时,电极④上质量变化______g, 电极⑥上质量变化______g。

(1)C池属于什么装置 。
(2)电极②上发生电极反应式为 ;B池中发生的总反应方程式为 。
(3)反应进行一段时间后,A、B、C三池中电解质溶液浓度基本不变的是________。
(4)当电路上有0.2 mol电子流过时,电极④上质量变化______g, 电极⑥上质量变化______g。
(1)电解精炼铜(电解池) (2)2H++2e- = H2↑ 4AgNO3+2H2O 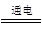 4Ag+4HNO3+O2↑
4Ag+4HNO3+O2↑
(3)C池 (4)21.6 6.4
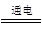 4Ag+4HNO3+O2↑
4Ag+4HNO3+O2↑(3)C池 (4)21.6 6.4
试题分析:(1)由图中电极材料及电解质溶液可判断B池为电解池,A池、C池符合原电池条件,但由于Ag-Zn活动性差别比Ag-Cu活动性差别大,所以Ag-Zn原电池更容易放电,若A池、C池相连则C池为电解池,C池符合电镀条件,因此C池为电镀池。(2)A池②极为原电池正负极,电极反应2H++2e- = H2↑,B池电解AgNO3溶液,总反应为4AgNO3+2H2O
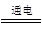 4Ag+4HNO3+O2↑;(3)C池是电镀池,电镀过程中电解质溶液的浓度不变。(4)电极④极发生: 2Ag++2e-=2Ag,电极⑥极发生:2Cu2++2e-=2Cu,由得失电子守恒可求出④、⑥电极上质量的变化;
4Ag+4HNO3+O2↑;(3)C池是电镀池,电镀过程中电解质溶液的浓度不变。(4)电极④极发生: 2Ag++2e-=2Ag,电极⑥极发生:2Cu2++2e-=2Cu,由得失电子守恒可求出④、⑥电极上质量的变化;
练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
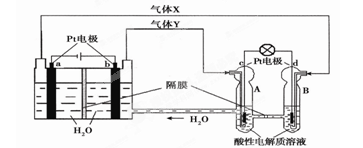
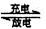 VO2++2H++V2+。下列叙述正确的是 ( )
VO2++2H++V2+。下列叙述正确的是 ( )
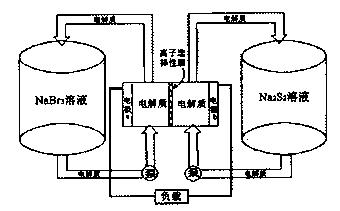
 Na2S4+3NaBr反应原理进行工作,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过。
Na2S4+3NaBr反应原理进行工作,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过。