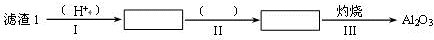题目内容
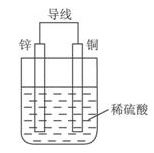
如下图所示,甲池的总反应式为:N2H4+O2=N2+2H2O

下列关于该电池工作时说法正确的是

下列关于该电池工作时说法正确的是
| A.甲池中负极反应为:N2H4-4e-=N2+4H+ |
| B.甲池溶液pH不变,乙池溶液pH减小 |
| C.甲池中消耗2.24L O2,此时乙池中理论上最多产生12.8g固体 |
| D.反应一段时间后,向乙池中加一定量CuO固体,能使CuSO4溶液恢复到原浓度 |
D
试题分析:A、甲池中原电池反应,对应的电极反应式是:正极O2+4e-+2H2O=4OH-,负极N2H4-4e-+4OH-=N2+4H2O,错误;B、甲池中因反应生成了水会使溶液的pH值减小,乙池中因反应生成了酸也会使溶液的pH值减小,错误;C、说气体的体积没有说标况无法计算,错误;D、乙池发生的是电解池反应两极析出的分别是Cu和O2,因而加CuO后溶液能够复原,正确。

练习册系列答案
相关题目

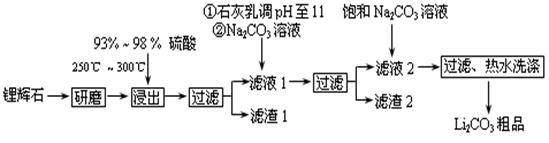
 Li2SO4 + Al2O3·4SiO2·H2O↓
Li2SO4 + Al2O3·4SiO2·H2O↓