题目内容
在密闭容器中,对于反应2NO2(g)?N2O4(g)△H<0,增大压强(体积迅速减小),下列说法正确的是 ( )
| A、平衡逆向移动 |
| B、混合气体颜色比原来深 |
| C、混合气体颜色比原来浅 |
| D、混合气体的平均相对分子质量变小 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:反应2NO2(g)?N2O4(g)△H<0,反应是气体体积减小的放热反应,增大压强平衡正向进行;
解答:
解:反应2NO2(g)?N2O4(g)△H<0,反应是气体体积减小的放热反应,增大压强平衡正向进行;
A、依据改变条件和平衡移动原理可知,平衡正向进行,故A错误;
B、增大压强,体积迅速减小,平衡移动程度不如体积减小带来的改变大,所以混合气体颜色加深,故B正确;
C、增大压强,体积迅速减小,平衡移动程度不如体积减小带来的改变大,所以混合气体颜色加深,故C错误;
D、增大压强,气体质量不变,物质的量减小,混合气体的平均相对分子质量变大,故D错误;
故选B.
A、依据改变条件和平衡移动原理可知,平衡正向进行,故A错误;
B、增大压强,体积迅速减小,平衡移动程度不如体积减小带来的改变大,所以混合气体颜色加深,故B正确;
C、增大压强,体积迅速减小,平衡移动程度不如体积减小带来的改变大,所以混合气体颜色加深,故C错误;
D、增大压强,气体质量不变,物质的量减小,混合气体的平均相对分子质量变大,故D错误;
故选B.
点评:本题考查了化学平衡移动原理的分析判断,注意反应特征和理解应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
在托盘天平的左右两边各放一个烧杯,加入足量盐酸并使天平保持平衡向左边烧杯中加入14.4g Mg,向右边烧杯中加入14.4g Al,此时天平不再平衡,下述可以使天平恢复平衡的是( )
| A、右边加0.45g Al |
| B、左边加0.98g Mg |
| C、左边加14.4g Mg,右边加15.3g Al |
| D、左边加14.4g Mg,右边加14.85g Al |
下列氯化物中,既能由金属和氯气直接反应得到,又能由金属和盐酸反应制得的是( )
| A、FeCl2 |
| B、AlCl3 |
| C、FeCl3 |
| D、CuCl2 |
下列说法中正确的是( )
| A、向沸水中滴加饱和FeCl3溶液有红褐色沉淀产生 |
| B、制备AlCl3、CuCl2均可以采用将溶液直接蒸干的方法 |
| C、Ksp数值越大的难溶电解质在水中的溶解能力不一定越强 |
| D、向碳酸钡沉淀中加入稀硫酸,沉淀发生转化,可推知硫酸钡的Ksp比碳酸钡的大 |
我国政府规定,国内销售的食盐必须加碘.关于加碘的下列叙述中不正确的是( )
| A、加碘食盐开袋后,不宜长期放置后食用 |
| B、加碘食盐中不能同时加碘化钾和碘酸钾 |
| C、加碘食盐中加入的是单质碘 |
| D、加碘食盐中加入是碘酸钾 |
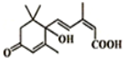 2012年广州市大街小巷对大量盆栽鲜花施用了诱抗素剂,以保证鲜花盛开,诱抗素的分子结构如图,下列关于该分子说法正确的是( )
2012年广州市大街小巷对大量盆栽鲜花施用了诱抗素剂,以保证鲜花盛开,诱抗素的分子结构如图,下列关于该分子说法正确的是( )| A、诱抗素含有碳碳双键、羟基、羰基、羧基 |
| B、诱抗素能与氯化铁溶液发生显色反应 |
| C、诱抗素能发生加成反应、水解反应、氧化反应 |
| D、1mol诱抗素在一定条件下可分别与4mol H2、2mol NaOH发生反应 |
2012年3月11日衡耒高速公路耒阳路段一辆运送化学物品的槽罐车侧翻,罐内15t苯泄入路边300m长的水渠,造成严重危险,许多新闻媒体进行了连续报道,以下报道中有科学性错误的是( )
| A、处理事故时,由于事故发生地周围比较空旷,有人提出用点火焚烧的办法来清除泄漏物,但由于苯燃烧会产生大量的黑烟扩大污染,所以该办法未被采纳 |
| B、由于苯是一种易挥发、易燃的物质,周围地区如果有一个火星就可能引起爆炸 |
| C、可以采取抽吸水渠中上层液体的办法,达到清除泄漏物的目的 |
| D、由于大量苯溶于水中渗入土壤,会对周边农田、水源造成严重污染 |
下列物质在水溶液中既能电离又能水解的是( )
| A、NH4Cl |
| B、NaHS |
| C、HNO3 |
| D、HClO |
下列实验设计或实验操作中,正确的是( )
A、 铜与浓硝酸反应制取NO2 |
B、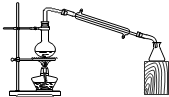 该装置设计合理,可实现石油的分馏 |
C、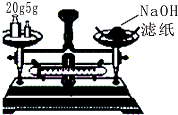 称量25g氢氧化钠 |
D、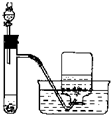 H2O2溶液与MnO2制备O2 |