题目内容
【题目】已知CaSO4受热分解,由于受热温度不同,气体成分也不同.气体成分可能为SO2、SO3和O2中的一种、二种或三种.某化学课外活动小组准备通过系列实验探究CaSO4分解生成的气体,进而确定CaSO4分解的化学方程式.
(1)[提出猜想]Ⅰ.所得气体的成分可能只含SO3一种;
Ⅱ.所得气体的成分可能含有二种;(填分子式)
(2)Ⅲ.所得气体的成分可能含有 SO2、SO3、O2三种.[设计实验]
该化学课外活动小组准备通过测定D装置的增重以及量筒中水的体积,来探究CaSO4分解生成的气体成分,进而确定CaSO4分解的化学方程式.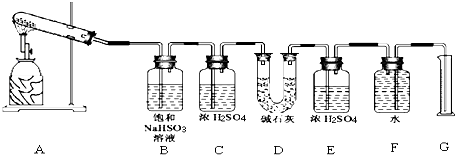
[实验过程]
根据上述实验方案进行试验.已知实验结束时,CaSO4完全分解.
请结合以下实验现象和记录的实验数据进行分析:
①若实验结束时,G中量筒没有收集到水,则证明猜想正确.(填Ⅰ或Ⅱ或Ⅲ)
②若实验结束时,装置D的总质量增加,能否断定气体产物中一定含有SO2而不含SO3?请说明理由: .
③该实验设计中,容易给测定带来较大误差的因素有 .
(写出一种即可)
④经改进后,有两组同学进行该实验,由于加热时的温度不同,实验测得数据也不同,
相关数据如下:
实验小组 | 称取CaSO4 | 装置D增加 | 量取气体体积的装置测量的气体体积 (折算成标准状况下气体的体积) (mL) |
一 | 4.08 | 2.56 | 224 |
二 | 5.44 | 2.56 | 448 |
请通过计算,推断第二组同学得出的CaSO4分解的化学反应方程式:
第二组: .
【答案】
(1)SO2、O2
(2)Ⅰ;不能,因为SO3与B中的饱和NaHSO3反应会生成等物质的量的SO2;排水量气法测定气体的体积时量筒和广口瓶中液面变化和压强变化对液体体积的读数会产生误差;2CaSO4 ![]() 2CaO+2SO2↑+O2↑
2CaO+2SO2↑+O2↑
【解析】解:(1)[提出猜想]Ⅱ.根据硫酸钙分解可能发生两种情况2CaSO4 ![]() 2CaO+2SO2↑+O2↑或 CaSO4
2CaO+2SO2↑+O2↑或 CaSO4 ![]() CaO+SO3↑,或者两个反应同时发生来判断,所得气体的成分可能只含 SO3一种,所得气体的成分可能含有SO2、O2 , 所得气体的成分可能含有 SO2、SO3、O2三种,所以答案是:SO2、O2;(2)[实验过程] ①若实验结束时装置G中量筒没有收集到水,说明生成的气体完全被吸收,因为生成二氧化硫时一定生成氧气,氧气不能被吸收,所以生成的气体只能是三氧化硫,所以I是正确的,故选I,所以答案是:Ⅰ;②若实验结束,经测定装置D的总质量增加了,二氧化硫和三氧化硫都是酸性氧化物,碱石灰可以吸收二氧化硫、三氧化硫,SO3与B中的饱和NaHSO3反应会生成等物质的量的SO2;所以答案是:不能,因为SO3与B中的饱和NaHSO3反应会生成等物质的量的SO2;③该实验设计中,容易给测定带来较大误差的因素有,排水量气法测定气体的体积时量筒和广口瓶中液面变化和压强变化对液体体积的读数会产生误差最大,所以答案是:排水量气法测定气体的体积时量筒和广口瓶中液面变化和压强变化对液体体积的读数会产生误差;④二组、设5.44g硫酸钙分解生成xmolSO3 , ymolSO2 , 则有
CaO+SO3↑,或者两个反应同时发生来判断,所得气体的成分可能只含 SO3一种,所得气体的成分可能含有SO2、O2 , 所得气体的成分可能含有 SO2、SO3、O2三种,所以答案是:SO2、O2;(2)[实验过程] ①若实验结束时装置G中量筒没有收集到水,说明生成的气体完全被吸收,因为生成二氧化硫时一定生成氧气,氧气不能被吸收,所以生成的气体只能是三氧化硫,所以I是正确的,故选I,所以答案是:Ⅰ;②若实验结束,经测定装置D的总质量增加了,二氧化硫和三氧化硫都是酸性氧化物,碱石灰可以吸收二氧化硫、三氧化硫,SO3与B中的饱和NaHSO3反应会生成等物质的量的SO2;所以答案是:不能,因为SO3与B中的饱和NaHSO3反应会生成等物质的量的SO2;③该实验设计中,容易给测定带来较大误差的因素有,排水量气法测定气体的体积时量筒和广口瓶中液面变化和压强变化对液体体积的读数会产生误差最大,所以答案是:排水量气法测定气体的体积时量筒和广口瓶中液面变化和压强变化对液体体积的读数会产生误差;④二组、设5.44g硫酸钙分解生成xmolSO3 , ymolSO2 , 则有
80x+64y=2.56
x+y= ![]() =0.04
=0.04
解之得:x=0,y=0.04mol,
又n(O2)= ![]() =0.02mol,所以二者的物质的量之比为2:1,方程式:2CaSO4
=0.02mol,所以二者的物质的量之比为2:1,方程式:2CaSO4 ![]() 2CaO+2SO2↑+O2↑;
2CaO+2SO2↑+O2↑;
所以答案是:2CaSO4 ![]() 2CaO+2SO2↑+O2↑.
2CaO+2SO2↑+O2↑.

【题目】下列实验现象描述正确的是
选项 | 实 验 | 现 象 |
A | 向氢氧化钠溶液中滴加FeCl3饱和溶液 | 有氢氧化铁胶体产生 |
B | 在酒精灯上加热铝箔 | 铝箔熔化,失去光泽,熔化的铝滴落下来 |
C | 向久置于空气中的FeSO4溶液中滴加NaOH溶液 | 立刻产生大量白色沉淀 |
D | 加热放在坩埚中的小块钠 | 钠先熔化成光亮的小球,燃烧时火焰为黄色,燃烧后生成淡黄色固体 |
A. A B. B C. C D. D