题目内容
【题目】对于在密闭容器中进行的可逆反应![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.容器内只含有![]() 、
、![]() 、
、![]() 三种分子
三种分子
B.![]() 只存在
只存在![]() 分子中
分子中
C.容器内含有![]() 、
、![]() 、
、![]() 等分子
等分子
D.反应达到限度时,所有物质的质量都相等
【答案】C
【解析】
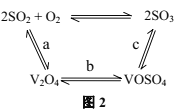
该反应为可逆反应,在混合气体中充入一定量的![]() ,
,![]() 和
和![]() 反应生成
反应生成![]() 中含有
中含有![]() ,同时
,同时![]() 分解生成
分解生成![]() 和
和![]() ,则
,则![]() 中含有
中含有![]() 原子,则
原子,则![]() 原子存在于
原子存在于![]() 、
、![]() 和
和![]() 中,根据可逆反应不会进行彻底,
中,根据可逆反应不会进行彻底,![]() 和
和![]() 在一定条件下,不会全部转化为三氧化硫,即生成三氧化硫的量小于2mol。
在一定条件下,不会全部转化为三氧化硫,即生成三氧化硫的量小于2mol。
A.反应达到限度时,达到平衡状态,容器内含有![]() 、
、![]() 、
、![]() 分子,还可能含有
分子,还可能含有![]() 、
、![]() 分子,故A错误;
分子,故A错误;
B.![]() 和
和![]() 反应生成
反应生成![]() 中含有
中含有![]() ,同时
,同时![]() 分解生成
分解生成![]() 和
和![]() ,
,![]() 原子存在于
原子存在于![]() 、
、![]() 和
和![]() 中,故B错误;
中,故B错误;
C.容器内含有![]() 、
、![]() 、
、![]() 等分子,故C正确;
等分子,故C正确;
D.反应达到限度时,所有物质的质量不再变化,但是不一定是相等的,故D错误;
故选:C。

 名校课堂系列答案
名校课堂系列答案【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据:
苯 | 溴 | 溴苯 | |
密度/g·cm﹣3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
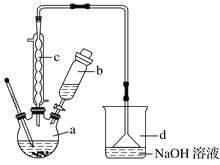
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,向a中滴入几滴溴,有白色烟雾产生,是因为生成了_______气体,继续滴加液溴滴完。铁屑的作用是___________;a中发生的化学反应方程式______________________。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是____;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_______;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为______,要进一步提纯,下列操作中必须的是______(填入正确选项前的字母);
A.重结晶B.过滤C.蒸馏D.萃取
(4)在该实验中,a的容积最适合的是_______(填入正确选项前的字母)。
A.25mL B.50mL C.250mL D.500mL
【题目】如图所示装置中观察到电流计指针偏转,M棒变粗,N棒变细,指针指向M,由此判断下表中所列M、N、P物质,其中可以成立的组合是( )
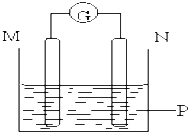
M | N | P | |
A | 锌 | 铜 | 稀硫酸溶液 |
B | 铜 | 铁 | 稀盐酸溶液 |
C | 银 | 锌 | 硝酸银溶液 |
D | 锌 | 铁 | 硝酸铁溶液 |
A.A B.B C.C D.D