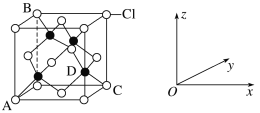
题目内容
【题目】近年来,以煤为原料制备的一些化工产品前景又被看好。下图是以烃A为原料生产人造羊毛的合成路线。下列说法正确的是
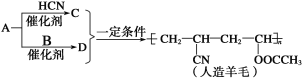
A.A生成C的反应属于加成反应B.合成人造羊毛的反应属于缩聚反应
C.A生成D的反应属于取代反应D.烃A的结构简式为CH2=CH2
【答案】A
【解析】
由人造羊毛的结构简式逆推,C、D的结构简式为CH2=CH-CN、CH3COOCH=CH2,A属于烃,结合A→C和A→D的反应,A为CH≡CH,C为CH2=CHCN,B为CH3COOH,D为CH3COOCH=CH2,据此分析解答
A.CH≡CH与HCN发生加成反应生成CH2=CHCN,故A正确;
B.一定条件下,CH2=CH-CN、CH3COOCH=CH2发生加聚反应生成人造羊毛,反应方程式为:nCH2=CH-CN+nCH3COOCH=CH2![]()
![]() ,无小分子生成,故B错误;
,无小分子生成,故B错误;
C. A→D的化学反应方程式:HC≡CH+CH3COOH![]() H2C=CH-OOCCH3,属于加成反应,故C错误;
H2C=CH-OOCCH3,属于加成反应,故C错误;
D.根据分析,烃A的结构简式为CH≡CH,故D错误;
答案选A。

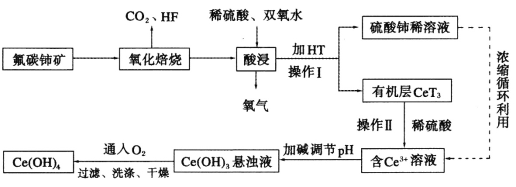
【题目】硫酸锌是一种重要的工业原料,广泛用于农业、化工、电镀等行业。工业上由锌渣(主要成分为ZnO、FeO、CuO、PbO等)等工业废料生产ZnSO4·7H2O的流程如下:
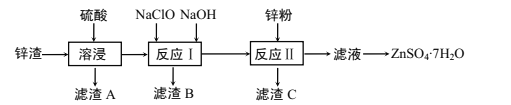
(1)“溶浸”操作中,选用“锌渣”而不选择氧化锌矿粉的原因是______;该操作中不断通入高温水蒸气的目的是________。
(2)“滤渣A”的主要成分是________。
(3)“反应Ⅰ”中,加入NaClO反应的离子方程式为___。
(4)“反应Ⅰ”中,再加入NaOH调节pH约为4.5,则“滤渣B”的主要成分是_____(填化学式)。(Ksp[Zn(OH)2]=3×10-17,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=2.8×10-39)
(5)“反应Ⅱ”中,加入的锌粉需用少量稀硫酸处理,原因是_________。
(6)取28.7gZnSO4·7H2O加热至不同温度,剩余固体的质量如下表:
温度/℃ | 100 | 250 | 680 | 930 |
质量/g | 17.90 | 16.10 | 13.43 | 8.10 |
则680℃时所得固体的化学式为_________(填字母标号)。
A.ZnO B.Zn3O(SO4)2 C.ZnSO4 D.ZnSO4·H2O
【题目】工业上“固定”和利用CO2能有效地减轻“温室效应”。
I.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H=-49.0kJmol﹣1,某科学实验将6molCO2和8 molH2充入一容积为2L的密闭容器中(温度保持不变),测得H2的物质的量随时间变化如下图中实线所示(图中字母后的数字表示对应的坐标):
CH3OH(g)+H2O(g) △H=-49.0kJmol﹣1,某科学实验将6molCO2和8 molH2充入一容积为2L的密闭容器中(温度保持不变),测得H2的物质的量随时间变化如下图中实线所示(图中字母后的数字表示对应的坐标):

回答下列问题:
(1)以下说法不正确的是(__________)
A.0~1min的平均反应速率大于3~4min的平均反应速率
B.达到平衡时H2的转化率为75%
C. 在其它条件不变时,若提高反应的温度正反应速率增大,逆反应速率减小
(2)该反应在0 ~8 min内CO2的平均反应速率是_______。
(3)该反应的平街常数K=______________。
(4)仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线所示。与实线相比,虚线I改变的条件可能是_________。若实线对应条件下平衡常数为K,虚线I对应条件下平衡常数为K1,虚线II对应条件下平衡常数为K2,则K、K1和K2的大小关系是____。
II.己知25℃时,乙酸和碳酸的电离平衡常数如下表:
物质的化学式 | CH3COOH | H2CO3 | |
电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 | K2=5.6×10-11 |
(1)用饱和氨水吸收CO2可得到NH4HCO3溶液,若已知CH3COONH4溶液pH=7,则(NH4)2CO3溶液显_____(填“酸性”、“碱性”或“中性”)。
(2)25℃时,在0.lmolL﹣1乙酸溶液中加入一定量的NaHCO3,保持温度不变,所得混合液的pH=6,那么混合液中![]() =_______;该混合溶液中的离子浓度由大到小的顺序为:________________。
=_______;该混合溶液中的离子浓度由大到小的顺序为:________________。