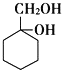
题目内容
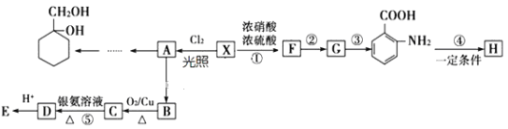
【题目】A(C2H4)是基本的有机化工原料,由A制备聚丙烯酸甲酯(有机玻璃主要成分)和肉桂酸的合成路线(部分反应条件略去)如图所示:
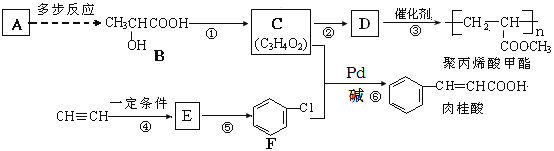
已知:①E的相对分子质量在70~80之间,步骤④的反应类型是加成反应
②![]() +CH2=CH2
+CH2=CH2![]() +HX (X为卤原子,R为取代基)
+HX (X为卤原子,R为取代基)
回答下列问题:
(1)F的名称是________;反应①的反应试剂和反应条件是________;⑥的反应类型是________。
(2)反式肉桂酸的结构简式为_________。
(3)由C制取D的化学方程式为_________。
(4)肉桂酸的同分异构体中能同时满足下列条件的共有_______种(不考虑立体异构);
①能与FeCl3溶液发生显色反应;
②能使溴的四氯化碳溶液褪色;
③能发生银镜反应。
其中苯环上只有两个取代基,核磁共振氢谱为6组峰、且峰面积比为2:2:1:1:1:1的是:________(写结构简式)。
(5)请运用所学知识并结合信息: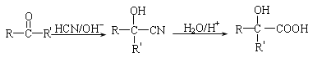 ,设设计由A(C2H4)制备B的合成路线(无机试剂任选):____________。
,设设计由A(C2H4)制备B的合成路线(无机试剂任选):____________。
【答案】氯苯 浓硫酸、加热 取代反应 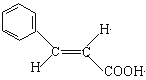 CH2=CHCOOH+CH3OH
CH2=CHCOOH+CH3OH![]() CH2=CHCOOCH3+H2O 16
CH2=CHCOOCH3+H2O 16 ![]() CH2=CH2
CH2=CH2![]() CH3CH2OH
CH3CH2OH![]() CH3CHO
CH3CHO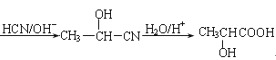 或CH2=CH2
或CH2=CH2![]() CH3CHO
CH3CHO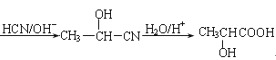
【解析】
A为CH2=CH2,B是乳酸,B发生消去反应生成C,C为CH2=CHCOOH,C与CH3OH发生酯化反应产生D:CH2=CHCOOCH3,D发生加聚反应生成聚丙烯酸甲酯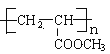 ; ①E的相对分子质量在70~80之间,步骤④的反应类型是加成反应,则E为
; ①E的相对分子质量在70~80之间,步骤④的反应类型是加成反应,则E为![]() ,苯发生取代反应生成F,由信息②C、F发生取代反应生成肉桂酸;
,苯发生取代反应生成F,由信息②C、F发生取代反应生成肉桂酸;
(5)由A(C2H4)制备B,由A(C2H4)制备CH3CH(OH)COOH,可以用乙烯与水加成得CH3CH2OH,CH3CH2OH氧化得CH3CHO,CH3CHO与HCN发生加成反应得CH3CH(OH)CN,CH3CH(OH)CN水解得CH3CH(OH)COOH。
根据上述分析可知A是CH2=CH2,C是CH2=CHCOOH,D是CH2=CHCOOCH3,E是![]() 。
。
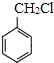
(1)根据F结构简式知,F的名称是氯苯,反应①乳酸在浓硫酸、加热条件下发生消去反应产生CH2=CH-COOH,为醇羟基发生的消去反应,所需的反应试剂和反应条件是;反应⑥是氯苯![]() 与丙烯酸CH2=CHCOOH发生取代反应产生肉桂酸
与丙烯酸CH2=CHCOOH发生取代反应产生肉桂酸![]() ;
;
(2)根据上述分析可知E是苯,结构简式为![]() ,反式肉桂酸是苯环与羧基在碳碳双键的不同侧,其结构简式为
,反式肉桂酸是苯环与羧基在碳碳双键的不同侧,其结构简式为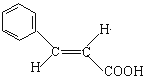 ;
;
(3)C是CH2=CHCOOH,D是CH2=CHCOOCH3,C发生酯化生成D为CH2=CH-COOCH3,由C制取D的化学方程式为CH2=CHCOOH+CH3OH CH2=CHCOOCH3+H2O;
CH2=CHCOOCH3+H2O;
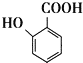
(4)肉桂酸结构简式为![]() ,其同分异构体中能同时满足下列条件:①能与FeCl3溶液发生显色反应,说明有酚羟基,②能使溴的四氯化碳溶液褪色,说明有碳碳不饱和键;③能发生银镜反应,说明有醛基,则符合条件的结构为苯环上连有-CH=CHCHO、-OH,或-C(CHO)=CH2、-OH,每种都有邻间对三种可能的结构,则有两个取代基的同分异构体种类有2×3=6种;也可以是苯环上连有-OH、-CHO、-CH=CH2三种取代基,根据定二动一的原则,有10种结构,所以共有6+10=16种,其中苯环上只有两个取代基,核磁共振氢谱为6组峰、且峰面积比为2:2:1:1:1:1的是
,其同分异构体中能同时满足下列条件:①能与FeCl3溶液发生显色反应,说明有酚羟基,②能使溴的四氯化碳溶液褪色,说明有碳碳不饱和键;③能发生银镜反应,说明有醛基,则符合条件的结构为苯环上连有-CH=CHCHO、-OH,或-C(CHO)=CH2、-OH,每种都有邻间对三种可能的结构,则有两个取代基的同分异构体种类有2×3=6种;也可以是苯环上连有-OH、-CHO、-CH=CH2三种取代基,根据定二动一的原则,有10种结构,所以共有6+10=16种,其中苯环上只有两个取代基,核磁共振氢谱为6组峰、且峰面积比为2:2:1:1:1:1的是![]() ;
;
(5)由A(C2H4)制备B,可以用CH2=CH2与水加成得CH3CH2OH,CH3CH2OH催化氧化得乙醛CH3CHO,CH3CHO与HCN发生加成反应得CH3CH(OH)CN,CH3CH(OH)CN发生水解反应得CH3CH(OH)COOH。故合成路线为CH2=CH2![]() CH3CH2OH
CH3CH2OH![]() CH3CHO
CH3CHO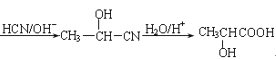 ;也可以是CH2=CH2直接催化氧化产生乙醛CH3CHO ,CH3CHO与HCN发生加成反应得CH3CH(OH)CN,CH3CH(OH)CN发生水解反应得CH3CH(OH)COOH,故合成路线也可以是CH2=CH2
;也可以是CH2=CH2直接催化氧化产生乙醛CH3CHO ,CH3CHO与HCN发生加成反应得CH3CH(OH)CN,CH3CH(OH)CN发生水解反应得CH3CH(OH)COOH,故合成路线也可以是CH2=CH2![]() CH3CHO
CH3CHO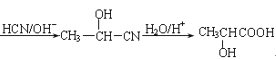 。
。

 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案