题目内容
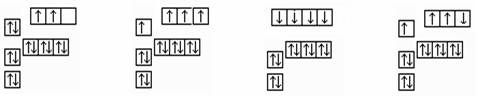
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态氢化物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁的最外层电子数和电子层数相等,则下列说法中正确的是 ( )
| A.原子半径:丙>乙>丁 |
| B.单质的还原性:丁>丙>甲 |
| C.甲、乙、丙的氧化物均为共价化合物 |
| D.乙、丙、丁的最高价氧化物对应的水化物能相互反应 |
D
解析试题分析:甲、乙、丙、丁四元素分别为:H、N、Na、Al。则四者的原子半径为:Na>Al>N>H;A选项不正确;单质的还原性:Na>Al>H2;B选项不正确;C选项丙的氧化物可能为Na2O或者Na2O2,都属于离子化合物,所以不正确,;D选项乙、丙、丁的最高价氧化物对应的水化物分别是HNO3、NaOH、Al(OH)3,NaOH是强碱,Al(OH)3是两性氢氧化物,HNO3是强酸。故它们的最高价氧化物对应的水化物能相互反应。正确。
考点:考查元素周期表和元素周期律的知识。

练习册系列答案
相关题目
原子序数在3~9之间的元素,随着核电荷数的递增而逐渐增大的是
| A.电子层数 | B.最外层电子数 | C.原子半径 | D.化合价 |
下列关于氢原子电子云图的说法正确的是
| A.通常用小黑点来表示电子的多少,黑点密度大,电子数目大 |
| B.黑点密度大,单位体积内电子出现的机会大 |
| C.通常用小黑点来表示电子绕核作高速圆周运动 |
| D.电子云图是对电子运动无规律性的描述 |
据下表信息,判断以下叙述正确的是( ) 部分短周期元素的原子半径及主要化合价
| 元素代号 | G | L | M | Q | R | T |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.104 | 0.075 | 0.066 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | +5、-3 | -2 |
A.GOH溶液和M(OH)3可以相互反应
B.非金属性:T<Q
C.气态氢化物的稳定性:R>T
D.L2+与T2-核外电子数相等
230Th和232Th是钍的两种同位素,232Th可以转化成233U。下列有关Th的说法正确的是
| A.Th 元素的质量数是232 | B.Th 元素的相对原子质量是231 |
| C.232Th 转换成233U是化学变化 | D.230Th和232Th的化学性质几乎相同 |
 、
、 、
、 、
、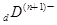 电子层结构相同。关于A、B、C、D四种元素叙述正确的是
电子层结构相同。关于A、B、C、D四种元素叙述正确的是