题目内容
据下表信息,判断以下叙述正确的是( ) 部分短周期元素的原子半径及主要化合价
| 元素代号 | G | L | M | Q | R | T |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.104 | 0.075 | 0.066 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | +5、-3 | -2 |
A.GOH溶液和M(OH)3可以相互反应
B.非金属性:T<Q
C.气态氢化物的稳定性:R>T
D.L2+与T2-核外电子数相等
AD
解析试题分析:从表中来看G、L、M元素的的原子半径都比较大依次减小,且都为正价,所以是金属元素。而Q、T元素都有-2价,所以推测是第六主族元素,根据半径可得Q、T分别为元素S、O,由此可推R是N,G、L、M则分别为Na、Mg、Al。所以NaOH溶液和Al(OH)3可以相互反应,A正确;O的非金属性强于S元素,B错误;O的非金属性同样强于N元素,所以对应的氢化物稳定性也要强,C错误;Mg 在第三周期,O在第二周期,所以形成的离子Mg 2+与O2- 都具有相同的电子层结构,核外电子数相同,D正确;故选AD。
考点:本题考查的是元素化合物的推断。

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
下表为元素周期表的一部分,有关说法正确的是
| 族 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | | ⑥ | ⑦ | | | ⑧ | |
A.④、⑤、⑥、⑦、①的原子半径依次减小
B.⑤、⑥、⑧的最高价氧化物对应的水化物不能相互反应
C.⑦、②、③、④的氢化物的稳定性依次增强
D.②、③的气态氢化物均能与它们的最高价氧化物对应的水化物反应
下列选项的说法中正确的是
| A.1s22s12p1表示的是激发态原子的电子排布 |
| B.3p2表示3p能级有两个原子轨道 |
| C.同一原子中,1s、2s、3s电子的能量逐渐减小 |
| D.同一原子中,2p、3p、4p能级的轨道数依次增多 |
某元素的一个原子形成的离子可表示为 ,下列说法正确的是
,下列说法正确的是
A. 含有的中子数为a+b 含有的中子数为a+b | B. 含有的电子数为a-n 含有的电子数为a-n |
| C.X原子的质量数为a+b+n | D.X原子的质量约为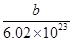 g g |
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态氢化物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁的最外层电子数和电子层数相等,则下列说法中正确的是 ( )
| A.原子半径:丙>乙>丁 |
| B.单质的还原性:丁>丙>甲 |
| C.甲、乙、丙的氧化物均为共价化合物 |
| D.乙、丙、丁的最高价氧化物对应的水化物能相互反应 |
能说明氯的非金属性比溴强的事实是( )
①共用电子对偏移程度:H-Cl > H-Br ②酸性:HClO4 > HBrO4
③热稳定性:HCl > HBr ④酸性:HCl <HBr
| A.①②③ | B.①②④ | C.②③④ | D.②③ |
短周期元素X、Y、Z、W、Q在周期表中的相对位置如图所示。下列说法不正确的是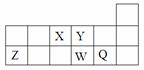
| A.离子半径的大小顺序为W>Q>Y>Z |
| B.X、Y、W三种元素的电负性大小顺序为X>Y>W |
| C.X、Z、W三种元素的最高价氧化物对应的水化物均能与强碱反应 |
| D.元素X的最简单氢化物与Q的氢化物化合的产物中既含共价键又含离子键 |
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是
| A.非金属性:Z<T<X |
| B.R与Q的电子数相差26 |
| C.气态氢化物稳定性:R <T<Q |
| D.最高价氧化物的水化物的酸性: X > T |
Rn+离子有m个电子,它的质量数为A,则原子核内的中子数为 ( )
| A.m +n | B.A-m+n | C.A-m-n | D.A+m-n |