题目内容
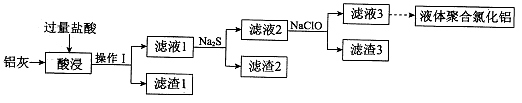
以铝灰(主要成分为Al、Al2O3,另有少量CuO、SiO2、FeO和Fe2O3杂质)为原料,可制得液体聚合氯化铝Alm(OH)nCl3m-n,生产的部分过程如下图所示(部分产物和操作已略去)。
已知某些硫化物的性质如下表:

(1)操作I是 。Al2O3与盐酸反应的离子方程式是 。
(2)滤渣2为黑色,该黑色物质的化学式是 。
(3)向滤液2中加入NaClO溶液至不再产生红褐色沉淀,此时溶液的pH约为3.7。NaClO的作用是 。
(4)将滤液3的pH调至4.2~4.5,利用水解反应得到液体聚合氯化铝。反应的化学方程式是 。
(5)将滤液3电解也可以得到液体聚合氯化铝。装置如图所示(阴离子交换膜只允许阴离子通过,电极为惰性电极)。

①写出阴极室的电极反应: 。
②简述在反应室中生成聚合氯他铝的原理: 。

已知某些硫化物的性质如下表:

(1)操作I是 。Al2O3与盐酸反应的离子方程式是 。
(2)滤渣2为黑色,该黑色物质的化学式是 。
(3)向滤液2中加入NaClO溶液至不再产生红褐色沉淀,此时溶液的pH约为3.7。NaClO的作用是 。
(4)将滤液3的pH调至4.2~4.5,利用水解反应得到液体聚合氯化铝。反应的化学方程式是 。
(5)将滤液3电解也可以得到液体聚合氯化铝。装置如图所示(阴离子交换膜只允许阴离子通过,电极为惰性电极)。

①写出阴极室的电极反应: 。
②简述在反应室中生成聚合氯他铝的原理: 。
(1)过滤 (2分)Al2O3+6H+=2Al3++3H2O (2分)
(2)CuS (2分)
(3)将Fe2+氧化为Fe3+,使转化为Fe(OH)3沉淀 (2分)
(4)mAlCl3+nH2O=Alm(OH)nCl3m-n+nHCl (写“ ”得分)(1分)
”得分)(1分)
(5)①2H++2e-=H2↑ (2分)
②电解过程中反应室中的Cl-通过阴离子交换膜进入阳极室,阴极室中的OH-通过阴离子交换膜进入反应室,生成聚合氯化铝。(2分)
(2)CuS (2分)
(3)将Fe2+氧化为Fe3+,使转化为Fe(OH)3沉淀 (2分)
(4)mAlCl3+nH2O=Alm(OH)nCl3m-n+nHCl (写“
 ”得分)(1分)
”得分)(1分)(5)①2H++2e-=H2↑ (2分)
②电解过程中反应室中的Cl-通过阴离子交换膜进入阳极室,阴极室中的OH-通过阴离子交换膜进入反应室,生成聚合氯化铝。(2分)
试题分析:(1)加入稀盐酸后,CuO、SiO2不溶于稀盐酸的杂质可过滤出,所以操作I是过滤;氧化铝与稀盐酸反应的离子方程式为Al2O3+6H+=2Al3++3H2O;
(2)根据硫化物的性质可知该黑色物质为CuS,因为硫化亚铁溶液稀盐酸中;
(3)加入次氯酸钠目的是把亚铁离子氧化成铁离子,转化为Fe(OH)3沉淀除去;
(4)根据聚合氯化铝的化学式和质量守恒定律,氯化铝水解的化学方程式为
mAlCl3+nH2O=Alm(OH)nCl3m-n+nHCl;
(5)①滤液3的主要成分是氯化铝,根据离子放电顺序,在阴极是阳离子放电,所以应为H+放电,电极反应为2H++2e-=H2↑;
②反应室两侧均为阴离子交换膜,电解过程中反应室中的Cl-通过阴离子交换膜进入阳极室,阴极室中OH-浓度增大,通过阴离子交换膜进入反应室,生成聚合氯化铝。

练习册系列答案
相关题目