题目内容
(18分)铁、铝与冷浓硫酸可发生钝化现象,故工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
[探究一]
(1)将已去除表面氧化物的铁钉(碳素钢)m g放入稀硫酸中,铁钉表面现象为 。取出铁钉用蒸馏水洗涤后干燥,置于冷浓硫酸中,10分钟后移入稀硫酸溶液中,观察,开始一段时间铁钉表面无明显变化,其原因是 。
(2)另称取铁钉放入足量冷浓硫酸中,加热,充分反应后,过滤得到、溶液X并收集到气体Y。
①甲同学认为X中除铁单质外外还可能含有Fe3+、Fe2+。若要确认其中的Fe2+,可选择试剂为_________________,现象是_______________________________________________。
②乙同学根据氧化还原反应原理,认为气体中必然含有SO2,取336ml(标准状况)气体Y通入足量溴水中,发生反应离子方程式为:________________________________________。
然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中SO2的体积分数为 。
[探究二]
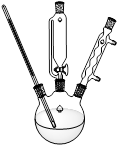
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含量有H2和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)加以验证。
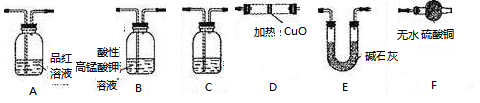
(3)装置的连接顺序是________________________________。
(4)除了C中的现象证明Q存在为,认为气体Y中还含有Q的理由是 (用化学方程式表示)。
(5)混合气体可能由H2、Q、SO2中的一种或多种气体组成,经测定其含氧量为50%,则该气体可能:①仅由SO2组成;②由H2和Q组成;③由H2和SO2组成;④由Q、SO2组成;⑤由H2、Q和SO2组成;其中可能正确的有( )
[探究一]
(1)将已去除表面氧化物的铁钉(碳素钢)m g放入稀硫酸中,铁钉表面现象为 。取出铁钉用蒸馏水洗涤后干燥,置于冷浓硫酸中,10分钟后移入稀硫酸溶液中,观察,开始一段时间铁钉表面无明显变化,其原因是 。
(2)另称取铁钉放入足量冷浓硫酸中,加热,充分反应后,过滤得到、溶液X并收集到气体Y。
①甲同学认为X中除铁单质外外还可能含有Fe3+、Fe2+。若要确认其中的Fe2+,可选择试剂为_________________,现象是_______________________________________________。
②乙同学根据氧化还原反应原理,认为气体中必然含有SO2,取336ml(标准状况)气体Y通入足量溴水中,发生反应离子方程式为:________________________________________。
然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中SO2的体积分数为 。
[探究二]
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含量有H2和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)加以验证。

(3)装置的连接顺序是________________________________。
(4)除了C中的现象证明Q存在为,认为气体Y中还含有Q的理由是 (用化学方程式表示)。
(5)混合气体可能由H2、Q、SO2中的一种或多种气体组成,经测定其含氧量为50%,则该气体可能:①仅由SO2组成;②由H2和Q组成;③由H2和SO2组成;④由Q、SO2组成;⑤由H2、Q和SO2组成;其中可能正确的有( )
| A.① | B.②③④ | C.①②⑤ | D.③④⑤ |
(1)有气泡冒出 铁钉表面被钝化(或其他合理答案)
(2)①酸性高锰酸钾溶液 酸性高锰酸钾溶液褪色 (或其他合理答案)
② SO2+Br2+H2O=4H++SO42-+2 Br - 66.7%
(3)B A C E D F E
(4)

(5)c
试题分析:
(1)铁钉(碳素钢)放入冷浓硫酸中,浓硫酸有较强的氧化性能使铁钉表面形成一层致密的氧化保护膜,阻止内层铁的进一步发生反应。
(2)Fe2+能使酸性的高锰酸钾褪色,溶液中已经有Fe3+,选择碱会造成干扰,氢氧化铁红褐色的颜色影响无法辨别氢氧化亚铁的白色沉淀是否生成。
(3)品红可以检验A中是否完全除去SO2
(4)
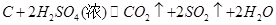
(5)经测定其含氧量为50%;氢气中不含氧元素;通过计算,CO2中氧元素的质量分数为72.7%,二氧化硫中氧元素的质量分数为50%.因此如果是一种物质就只能是二氧化硫,①可能正确;如果是两种物质,由H2和SO2组成时,小于50%,③不正确;只能是由H2和CO2组成,②可能正确;由CO2、SO2组成,大于50%,④不正确。由H2、CO2和SO2三种物质组成,⑤可能正确。故选C

练习册系列答案
相关题目