题目内容
13.能正确表示下列化学反应的离子方程式的是( )| A. | 氢氧化钡溶液与硫酸的反应OH-+H+═H2O | |
| B. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+═Cu2++Ag | |
| D. | 碳酸钙溶于稀盐酸中 CaCO3+2H+═Ca2++H2O+CO2↑ |
分析 A.氢氧化钡与硫酸反应生成硫酸钡沉淀和水,漏掉了生成水的反应;
B.澄清石灰水中,氢氧化钙应该拆开,不能保留化学式;
C.离子方程式两边正电荷不相等,不满足电荷守恒;
D.碳酸钙与盐酸反应生成氯化钙、二氧化碳气体和水.
解答 解:A.氢氧化钡与稀硫酸反应生成硫酸钡和水,正确的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故A错误;
B.澄清石灰水中的氢氧化钙应该拆开,正确的离子方程式为:OH-+H+═H2O,故B错误;
C.铜片插入硝酸银溶液中,离子方程式必须满足电荷守恒,正确的离子方程式为:Cu+2Ag+═Cu2++2Ag,故C错误;
D.碳酸钙溶于稀盐酸中,反应生成氯化钙、二氧化碳气体和水,反应的离子方程式为:CaCO3+2H+═Ca2++H2O+CO2↑,故D正确;
故选D.
点评 本题考查了离子方程式的判断,为高考中的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
3.目前人类已发现的非金属元素除稀有气体外共有16种,下列对这16种非金属元素的相关判断:①都是主族元素,最外层电子数都大于4;②单质在反应中都只能作氧化剂;③氢化物常温下都是气态,所以又都叫气态氢化物;④氧化物常温下都可以与水反应生成酸,其中正确的有( )
| A. | ①② | B. | ①③ | C. | ④ | D. | 均不正确 |
4.下列混合物的分离方法不正确的是( )
| A. | 酒精与水-蒸馏 | B. | 油与水-分液 | C. | 食盐与水-蒸发 | D. | KNO3与NaCl-过滤 |
1.下列化学反应的离子方程式正确的是( )
| A. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 往FeCl3溶液中加入Fe粉:2Fe3++Fe═3Fe2+ | |
| C. | 硅酸钠与盐酸反应:SiO32-+2H+═H2 SiO3↓ | |
| D. | 三氧化硫与氢氧化钙溶液的反应:SO3 +2OH-═SO42-+H2O |
8.关于SO2和Cl2的叙述错误的是( )
| A. | 都是大气污染物 | B. | 都可以用碱石灰干燥 | ||
| C. | 都能给NaOH溶液吸收 | D. | 都可以用向上排空气法收集 |
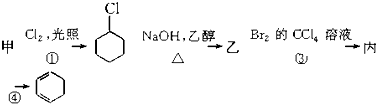
18.用有机物甲可制备环己二烯( ),其反应路线如图所示,下列有关判断正确的是( )
),其反应路线如图所示,下列有关判断正确的是( )
 ),其反应路线如图所示,下列有关判断正确的是( )
),其反应路线如图所示,下列有关判断正确的是( )
| A. | 甲的化学名称是苯 | |
| B. | 乙的结构简式为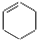 | |
| C. | 反应①为加成反应 | |
| D. | 有机物丙既能发生加成反应,又能发生取代反应 |
2.某同学在常温下设计以下实验流程探究Na2S203的化学性质.
pH=8$\stackrel{①}{\underset{\;←}{pH试纸}}$Na2S2O3溶液$→_{同时加过量BaCl_{2}溶液}^{②加入足量氯水}$白色沉淀B.
下列说法正确的是( )
pH=8$\stackrel{①}{\underset{\;←}{pH试纸}}$Na2S2O3溶液$→_{同时加过量BaCl_{2}溶液}^{②加入足量氯水}$白色沉淀B.
下列说法正确的是( )
| A. | 实验①说明Na2S2O3溶液中水电离的c(OH-)=10-8mol/L | |
| B. | Na2S2O3溶液PH=8的原因用离子方程式表示为S2O32-+2H2O═H2S2O3+2OH- | |
| C. | 生成的沉淀BaSO3或BaSO4,要进一步确认还需再加入稀硝酸验证 | |
| D. | 实验②说明Na2S2O3具有还原性 |
8.一定温度下向2L恒溶密闭容器中加入0.2molNO和0.1molCl2,发生反应2NO(g)+Cl2(g)?2ClNO(g)△H,10min后反应达到平衡,测得n(Cl2)=2.5×10-2mol.下列说法错误的是( )
| A. | 0-10min的平均反应速率:n(ClNO)=7.5×10-3mol•L-1•min-1 | |
| B. | 平衡时NO的转化率为75% | |
| C. | 其它条件保持不变,反应若在恒压条件下进行,平衡时NO的转化率变大 | |
| D. | 升高温度,反应的平衡常数减小,则△H>0 |