题目内容
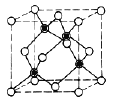
【题目】如图所示是金刚石的晶胞结构,除顶点和面心上有碳原子外,4条体对角线的1/4处还各有1个碳原子。回答下列问题:

(1)若图中原子1的坐标为![]() ,则原子2的坐标为________。若金刚石的晶胞参数为
,则原子2的坐标为________。若金刚石的晶胞参数为![]() ,则其中碳碳键的键长
,则其中碳碳键的键长![]() ________pm(用含
________pm(用含![]() 的代数式表示)。
的代数式表示)。
(2)面心立方![]() 晶胞与金刚石结构类似,阴、阳离子各占晶胞所含微粒数的一半。
晶胞与金刚石结构类似,阴、阳离子各占晶胞所含微粒数的一半。
①S元素及其同周期的相邻元素第一电离能由小到大的顺序是________,二氯化硫(![]() )分子中S原子的杂化类型是________。
)分子中S原子的杂化类型是________。
②写出基态![]() 的电子排布式________;把晶胞示意图中表示
的电子排布式________;把晶胞示意图中表示![]() 的小球全部涂黑_______。
的小球全部涂黑_______。
③锌锰干电池中![]() 可吸收电池反应产生的
可吸收电池反应产生的![]() 生成
生成![]() ,该离子中含有________个
,该离子中含有________个![]() 键。
键。
④若该![]() 晶胞的晶胞参数为
晶胞的晶胞参数为![]() ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为![]() ,则晶体的密度为________
,则晶体的密度为________![]() (列出计算式)
(列出计算式)
(3)有人设想冰的晶胞也应该类似于金刚石,但实际较为复杂,可能是因为氢键较弱而导致“饱和性和方向性”很难被严格执行。例如有文献报道氨晶体中每个氢原子都形成氢键,则每个![]() 与周围________个
与周围________个![]() 通过氢键相结合。
通过氢键相结合。
【答案】![]()
![]()
![]()
![]()
![]()
 或
或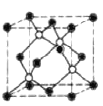 16
16 ![]() 6
6
【解析】
(1)若图中原子1的坐标为(0,0,0),则可建立以原子1为原点的坐标系,根据题干信息可知,原子2位于其中一条对角线上,根据立体几何可知,原子2的坐标为(![]() ,
,![]() ,
,![]() ,),晶胞中C原子形成的碳碳单键的键长刚好为体对角线的
,),晶胞中C原子形成的碳碳单键的键长刚好为体对角线的![]() ,因此,若金刚石的晶胞参数为
,因此,若金刚石的晶胞参数为![]() ,则其中碳碳键的键长为
,则其中碳碳键的键长为![]() pm,故答案为:(
pm,故答案为:(![]() ,
,![]() ,
,![]() ,);
,);![]() ;
;
(2)①与S元素同周期的相邻元素分别为P和Cl,一般情况下,同周期第一电离能逐渐增大,但P的3p轨道为3p3半充满状态,故第一电离能由小到大的为顺序为S<P<Cl,SCl2分子的中心原子的价电子对数为![]() ,则该分子的杂化方式为sp3杂化,故答案为:S<P<Cl;sp3;
,则该分子的杂化方式为sp3杂化,故答案为:S<P<Cl;sp3;
②基态Zn原子为30号元素,核外共有30个电子,而Zn2+失去了两个电子,其核外电子排布式为排布式为[Ar]3d10,ZnS晶胞与金刚石的结构类似,阴、阳离子各占晶胞所含微粒数的一半,则Zn2+可位于晶胞的顶点和面心或直接位于晶胞的体心,故答案为:[Ar]3d10; 或
或 ;
;
③[Zn(NH3)4]2+离子中Zn2+和NH3形成了4个配位键,同时1个NH3中N和H形成3个共价键,则该离子中共含有4+3×4=16个![]() 键,故答案为:16;
键,故答案为:16;
④由②分析可知,1个ZnS晶胞中共由4个ZnS,则晶胞的质量m为![]() ,晶胞的体积V=(a2×10-10)3=a23×10-30cm3,根据密度公式可得该晶体的密度
,晶胞的体积V=(a2×10-10)3=a23×10-30cm3,根据密度公式可得该晶体的密度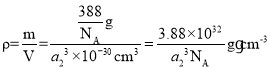 ,故答案为:
,故答案为:![]() ;
;
(3)若氨晶体中每个氢原子都形成氢键,则1个NH3中3个H原子与其他的NH3分子的N原子形成3个氢键,N原子与其他NH3分子的H原子形成3个氢键,则每个NH3与周围6个NH3通过氢键相结合,故答案为:6。

 名校课堂系列答案
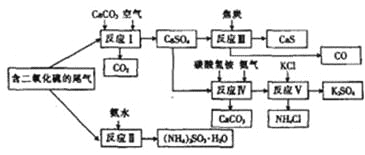
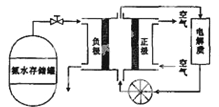
名校课堂系列答案【题目】二氧化氯(ClO2)广泛应用于纸浆漂白、杀菌消毒和水净化处理等领域。工业上利用甲醇还原NaClO3的方法制备ClO2,工艺流程如下:
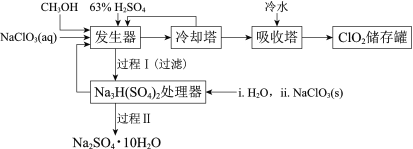
已知:a.发生器中制备ClO2的反应:12NaClO3+8H2SO4+3CH3OH= 12ClO2↑+3HCOOH+4Na3H(SO4)2↓+9H2O
b.相关物质的熔沸点:
物质 | CH3OH | HCOOH | ClO2 |
熔点/℃ | -97 | 9 | -59 |
沸点/℃ | 65 | 101 | 11 |
(1)ClO2可用于纸浆漂白、杀菌消毒是因其具有______性。
(2)冷却塔用于分离ClO2并回收CH3OH,应控制的最佳温度为______(填字母)。
A.0~10℃ B.20~30℃ C.60~70℃
(3)经过程Ⅰ和过程Ⅱ可以获得芒硝(Na2SO4·10H2O)并使部分原料循环利用。
已知:Na2SO4·10H2O和Na2SO4的溶解度曲线如下图:
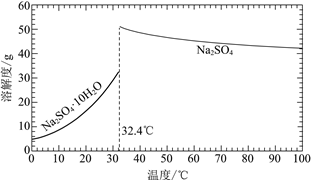
①Na3H(SO4)2处理器中获得芒硝时需加入NaClO3固体,从芒硝溶解平衡的角度解释其原因:______。
②结合Na2SO4·10H2O和Na2SO4的溶解度曲线,过程Ⅱ的操作是:在32.4℃恒温蒸发,______。
③Na3H(SO4)2处理器的滤液中可以循环利用的原料是NaClO3和______。