题目内容
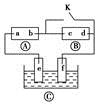
以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是
| A.未通电前上述镀锌装置可构成原电池,电镀过程是该原电池的充电过程 |
| B.因部分电能转化为热能,电镀时通过的电量与锌的析出量无确定关系 |
| C.电镀时保持电流恒定,升高温度不改变电解反应速率 |
| D.镀锌层破损后对铁制品失去保护作用 |
C
电镀时,通常把待镀的金属制品作阴极,把镀层金属作阳极,用含有镀层金属离子的溶液作电镀液。因此在铁制品上镀锌时,铁作阴极,锌作阳极,由于锌比铁活泼,因此未通电前可以构成原电池,但此时锌作负极失去电子,铁作正极,而电镀是锌仍然失电子,所以选项A不正确;在氧化还原反应中必需满足得失电子守恒,因此电镀时通过的电量与锌的析出量有确定关系而与能量变化无关,B不正确;由于电镀时保持电流恒定,因此导线中通过的电子速率是不变的,所以升高温度不能改变电解反应速率,C正确;镀锌层破损后,由于锌比铁活泼,所以即使发生电化学腐蚀也是锌失去电子而保护了铁,即选项D也不正确。

练习册系列答案
相关题目
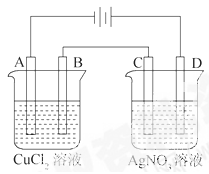
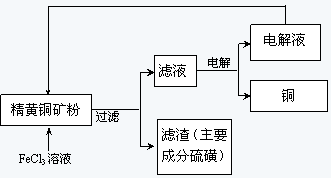

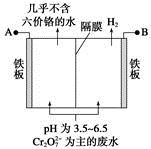
 ,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是
,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是