题目内容
20.下列离子方程式书写正确的是( )| A. | 向沸水中滴加饱和FeCl3溶液制胶体:Fe3++3H2O═Fe(OH)3(胶体)+3H+ | |
| B. | Ba(OH)2溶液与稀H2SO4混合:2H++2OH-═2H2O | |
| C. | 少量铁粉加入稀硝酸中:Fe+NO3-+4H+═Fe2++NO↑+2H2O | |
| D. | 钠放入水中:Na+H2O═Na++OH-+H2↑ |
分析 A.铁离子加入沸水中生成氢氧化铁胶体;
B.反应生成硫酸钡沉淀和水,漏掉了生成硫酸钡沉淀的反应;
C.铁粉少量,反应生成铁离子,不会生成亚铁离子;
D.2mol钠完全反应生成1mol氢气,该离子方程式不满足电子守恒.
解答 解:A.向沸水中滴加饱和FeCl3溶液制胶体,反应的离子方程式为:Fe3++3H2O═Fe(OH)3(胶体)+3H+,故A正确;
B.氢氧化钡与稀硫酸反应生成硫酸钡沉淀和水,正确的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故B错误;
C.少量铁粉加入稀硝酸中,反应生成硝酸铁、一氧化氮气体和水,正确的离子方程式为:Fe+NO3-+4H+═Fe3++NO↑+2H2O,故C错误;
D.钠与水反应生成氢氧化钠和氢气,正确的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,故D错误;
故选A.
点评 本题考查了离子方程式的书写判断,为高考中的高频题,题目难度中等,明确发生反应的实质为解答关键,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等),试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
11.实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH $→_{170℃}^{H_{2}SO_{4}浓}$ CH2=CH2,CH2=CH2+Br2→BrCH2CH2Br.用少量的溴和足量的乙醇制备l,2-二溴乙烷的装置如图:
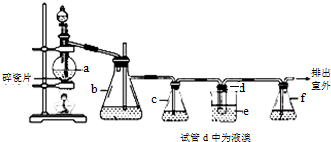
有关数据列表如下:
回答下列问题:
(1)在装置c中应加入③(选填序号),其目的是吸收反应中可能生成的酸性气体.
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)判断d管中制备二溴乙烷反应已结束的最简单方法是溴的颜色完全褪去.
(3)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的(填“上”或“下”)下层.
(4)若产物中有少量未反应的Br2,最好用②(填正确选项前的序号)洗涤除去.
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e),其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但不用冰水进行过度冷却,原因是:1,2-二溴乙烷的凝固点较低,过度冷却会使其凝固而使气路堵塞
(6)以1,2-二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2-二溴乙烷通过( ①)反应制得( ②),②通过( ③)反应制得氯乙烯,由氯乙烯制得聚氯乙烯.
①消去反应(填反应类型) ② (填该物质的电子式)③加成反应(填反应类型)写出第一步的化学方程式
(填该物质的电子式)③加成反应(填反应类型)写出第一步的化学方程式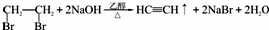 .
.

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在装置c中应加入③(选填序号),其目的是吸收反应中可能生成的酸性气体.
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)判断d管中制备二溴乙烷反应已结束的最简单方法是溴的颜色完全褪去.
(3)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的(填“上”或“下”)下层.
(4)若产物中有少量未反应的Br2,最好用②(填正确选项前的序号)洗涤除去.
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e),其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但不用冰水进行过度冷却,原因是:1,2-二溴乙烷的凝固点较低,过度冷却会使其凝固而使气路堵塞
(6)以1,2-二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2-二溴乙烷通过( ①)反应制得( ②),②通过( ③)反应制得氯乙烯,由氯乙烯制得聚氯乙烯.
①消去反应(填反应类型) ②
 (填该物质的电子式)③加成反应(填反应类型)写出第一步的化学方程式
(填该物质的电子式)③加成反应(填反应类型)写出第一步的化学方程式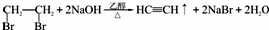 .
.
8.研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式,以下用于研究有机物的方法错误的是( )
| A. | 蒸馏常用于分离提纯液态有机混合物 | |
| B. | 对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团 | |
| C. | 燃烧法是研究确定有机物成分的有效方法 | |
| D. | 核磁共振氢常用于分析有机物的相对分子质量 |
15.下列除去杂质的操作中,能达到目的是( )
| A. | 除去苯中的少量溴:加入CCl4萃取后分液 | |
| B. | 除去乙烷中的乙烯:通入酸性高锰酸钾溶液中 | |
| C. | 除去CO2中的少量HCl气体:通过盛有饱和Na2CO3溶液的洗气瓶 | |
| D. | 除去FeCl2溶液中的少量FeCl3:加入足量Fe粉后过滤 |
5.下列排列顺序不正确的是( )
| A. | 热稳定性:HF>HCl>HBr | B. | 酸性:H3PO4>H2SO4>HClO4 | ||
| C. | 原子半径:Na>S>O | D. | 元素金属性:Na>Mg>Al |
12.短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同,X的一种核素在考古时常用来鉴定一些文物的年代,工业采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子,根据以上叙述,下列说法中正确的是( )
| A. | 上述四种元素的原子半径大小为W<X<Y | |
| B. | W、X、Y、Z原子的核外最外层电子数的总和为20 | |
| C. | 由W和Y元素组成的化合物不止一种 | |
| D. | 由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
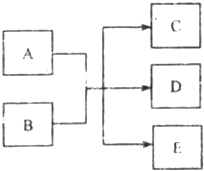 一定条件下,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.
一定条件下,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.