题目内容
【题目】现有下列物质:①稀硫酸 ②氧化铝固体 ③氨水 ④二氧化碳 ⑤FeCl3固体 ⑥稀NaOH溶液,按要求填空:
(1)上述物质中属于电解质的物质序号为______ ;
(2)有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是______;
(3)加入盐酸、NaOH溶液均能发生化学反应的物质序号为______;试用离子方程式说明:_______________、______________;
(4)能导电的物质序号为_______________;
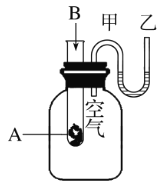
(5)实验室用⑤制备胶体的化学方程式为_______________________。
【答案】②⑤ ①⑥ ② Al2O3+6H+==2Al3++3H2O Al2O3+2OH-==2AlO2-+H2O ③⑥ FeCl3+3H2O![]() Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
【解析】
(1)电解质:在水溶液中或熔融状态下能导电的化合物;例:酸、碱、盐,金属氧化物等;
非电解质:在水溶液中和熔融状态下不能导电的化合物;例:有机物,非金属氧化物等;
(2)H++OH-=H2O可以表示强酸与可溶性强碱反应生成可溶性盐和水;
(3)两性物质,弱酸的酸式盐,弱酸的铵盐,铝,氨基酸,蛋白质既能与盐酸又能与氢氧化钠反应,酸性环境下硝酸根离子能氧化二价铁离子;
(4)物质导电的条件:存在自由电子,或者存在自由移动的离子;
(5)依据氯化铁水解性质解答;
(1)电解质:在水溶液中或熔融状态下能导电的化合物;例:酸、碱、盐,金属氧化物等;
非电解质:在水溶液中和熔融状态下不能导电的化合物;例:有机物,非金属氧化物等;
故答案为:②⑤;
(2)H++OH-=H2O可以表示强酸与可溶性强碱反应生成可溶性盐和水;
故答案为:①⑥;
(3)两性物质,弱酸的酸式盐,弱酸的铵盐,铝,氨基酸,蛋白质既能与盐酸又能与氢氧化钠反应,酸性环境下硝酸根离子能氧化二价铁离子,故给出的物质中既能与盐酸反应又能与氢氧化钠溶液反应是氧化铝,离子方程式是Al2O3+6H+==2Al3++3H2O ;Al2O3+2OH-==2AlO2-+H2O;
故答案为:②;Al2O3+6H+==2Al3++3H2O ;Al2O3+2OH-==2AlO2-+H2O;
(4)物质导电的条件:存在自由电子,或者存在自由移动的离子,
故答案为:③⑥;
(5)实验室向沸水中加入饱和氯化铁溶液来制备氢氧化铁胶体,其化学方程式为:FeCl3+3H2O![]() Fe(OH)3(胶体)+3HCl;
Fe(OH)3(胶体)+3HCl;
故答案为:FeCl3+3H2O![]() Fe(OH)3(胶体)+3HCl。
Fe(OH)3(胶体)+3HCl。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】[化学一选修3:物质结构与性质
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Ti3+的未成对电子数有__________个。
②LiBH4由Li+和BH4-构成,BH4-的空间构型是__________,B原子的杂化轨道类型是_____。
③某储氢材料是第三周期金属元素M的氢化物,M的部分电离能如下表所示:
I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
M是_______(填元素符号),判断理由为_______________。
(2)铜晶体中铜原子的堆积方式如图所示,铜晶体中原子的堆积模型属于____________。

(3)A原子的价电子排布式为3s23p5,铜与A 形成化合物的晶胞如图所示(黑点代表铜原子)。
①该晶体的化学式为______________。
②该化合物难溶于水但易溶于氨水,其原因是_____________ ,此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为____________。
③己知该晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,己知该晶体中Cu原子和A原子之间的最短距离为体对角线的1/4,则该晶体中Cu原子和A原子之间的最短距离为________pm。
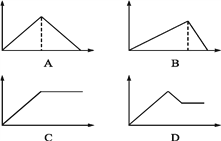
【题目】如图图象中,纵坐标为沉淀物的物质的量,横坐标为向溶液中加入反应物的物质的量,则相应的图像序号与(1)—(4)对应的是
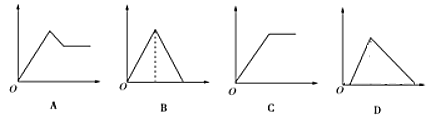
溶液 | 加入物质 | 对应的图像 |
(1)饱和石灰水 | 通过量CO2气体 | ____ |
(2)氯化铝溶液 | 加入过量氨水 | ____ |
(3)MgCl2、AlCl3的混合液 | 逐滴加入NaOH溶液至过量 | ____ |
(4)含少量NaOH的NaAlO2溶液 | 逐滴加入稀盐酸 | ____ |