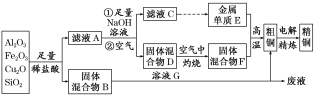
ЬтФПФкШн
ЁОЬтФПЁПМзДМЪЧвЛжжаТаЭШМСЯЃЌМзДМШМСЯЕчГиМДНЋДгЪЕбщЪвзпЯђЙЄвЕЛЏЩњВњЁЃЙЄвЕЩЯвЛАувдCOКЭH2ЮЊдСЯКЯГЩМзДМЃЌИУЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊЃК CO(g)+ 2H2(g)![]() CH3OH(g) ЁїH1ЃНЃ116 kJЁЄmolЃ1
CH3OH(g) ЁїH1ЃНЃ116 kJЁЄmolЃ1
ЃЈ1ЃЉвбжЊЃК![]() ЁїH2ЃНЃ283 kJЁЄmolЃ1
ЁїH2ЃНЃ283 kJЁЄmolЃ1
![]() ЁїH3ЃНЃ242 kJЁЄmolЃ1
ЁїH3ЃНЃ242 kJЁЄmolЃ1
дђБэЪО1molЦјЬЌМзДМЭъШЋШМЩеЩњГЩCO 2КЭЫЎеєЦјЪБЕФШШЛЏбЇЗНГЬЪНЮЊЃК
_______________________________________________ЃЛ
ЃЈ2ЃЉдкШнЛ§ЮЊ1LЕФКуШнШнЦїжаЃЌЗжБ№баОПдк230ЁцЁЂ250ЁцЁЂ 270ЁцШ§жжЮТЖШЯТКЯГЩМзДМЕФЙцТЩЁЃгвЭМЪЧЩЯЪіШ§жжЮТЖШЯТВЛЭЌЕФH2КЭCOЕФЦ№ЪМзщГЩБШЃЈЦ№ЪМЪБCOЕФЮяжЪЕФСПОљЮЊ1molЃЉгыCOЦНКтзЊЛЏТЪЕФЙиЯЕЁЃЧыЛиД№ЃК
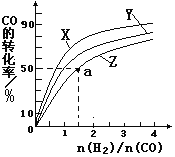
ЂйдкЩЯЪіШ§жжЮТЖШжаЃЌЧњЯпZЖдгІЕФЮТЖШЪЧ__________
ЂкРћгУЭМжаaЕуЖдгІЕФЪ§ОнЃЌМЦЫуГіЧњЯпZдкЖдгІЮТЖШЯТCO(g)+ 2H2(g) ![]() CH3OH(g)ЕФЦНКтГЃЪ§K=_____________________ЁЃ
CH3OH(g)ЕФЦНКтГЃЪ§K=_____________________ЁЃ
ЃЈ3ЃЉдкФГЮТЖШЯТЃЌНЋвЛЖЈСПЕФCOКЭH2ЭЖШы10LЕФУмБеШнЦїжаЃЌ5minЪБДяЕНЦНКтЃЌИїЮяжЪЕФЮяжЪЕФХЈЖШ(molL-1)БфЛЏШчЯТБэЫљЪОЃК
0min | 5min | 10min | |
CO | 0.1 | 0.05 | |
H2 | 0.2 | 0.2 | |
CH3OH | 0 | 0.04 | 0.05 |
Шє5minЁЋ10minжЛИФБфСЫФГвЛЬѕМўЃЌЫљИФБфЕФЬѕМўЪЧ_________________________ЃЛЧвИУЬѕМўЫљИФБфЕФСПЪЧ_______________ЁЃ
ЁОД№АИЁПCH3OH(g)+3/2O2(g)== CO2(g)+ 2H2O(g) ЁїHЃНЃ651kJЁЄmol-1270Ёц4 L2 /mol2діДѓH2ЕФХЈЖШдіДѓСЫ0.1 molL-1
ЁОНтЮіЁП
(1) ЂйCO(g)+ 2H2(g)![]() CH3OH(g) ЁїH1ЃНЃ116 kJЁЄmolЃ1ЃЛЂквбжЊЃК
CH3OH(g) ЁїH1ЃНЃ116 kJЁЄmolЃ1ЃЛЂквбжЊЃК![]() ЁїH2ЃНЃ283 kJЁЄmolЃ1ЃЛЂл
ЁїH2ЃНЃ283 kJЁЄmolЃ1ЃЛЂл![]() ЁїH3ЃНЃ242 kJЁЄmolЃ1ЃЌИљОнИЧЫЙЖЈТЩЗжЮіЃЌНЋЗНГЬЪННјааМЦЫуЃЌЙЋЪНЮЊ--Ђк+ЂлЁС2-ЂйМДПЩЕУШШЛЏбЇЗНГЬЪНЮЊЃК
ЁїH3ЃНЃ242 kJЁЄmolЃ1ЃЌИљОнИЧЫЙЖЈТЩЗжЮіЃЌНЋЗНГЬЪННјааМЦЫуЃЌЙЋЪНЮЊ--Ђк+ЂлЁС2-ЂйМДПЩЕУШШЛЏбЇЗНГЬЪНЮЊЃК
CH3OH(g)+3/2O2(g)== CO2(g)+ 2H2O(g) ЁїHЃН-283-242ЁС2+116=Ѓ651kJЁЄmol-1 ЃЛ
(2)ИљОнЗДгІCO(g)+ 2H2(g)![]() CH3OH(g) ЁїH1ЃНЃ116 kJЁЄmolЃ1ЗжЮіЃЌИУЗДгІЮЊЗХШШЗДгІЃЌЮТЖШдНИпЃЌзЊЛЏТЪдНЕЭЃЌЫљвдЧњЯпZЖдгІЕФЮТЖШЪЧ 270ЁцЃЛ
CH3OH(g) ЁїH1ЃНЃ116 kJЁЄmolЃ1ЗжЮіЃЌИУЗДгІЮЊЗХШШЗДгІЃЌЮТЖШдНИпЃЌзЊЛЏТЪдНЕЭЃЌЫљвдЧњЯпZЖдгІЕФЮТЖШЪЧ 270ЁцЃЛ
(3) CO(g)+ 2H2(g)![]() CH3OH(g) ЃЌИУЗДгІЕФЦНКтГЃЪ§K=
CH3OH(g) ЃЌИУЗДгІЕФЦНКтГЃЪ§K= ![]() ЃЌaЕуЪБЃЌвЛбѕЛЏЬМЕФзЊЛЏТЪЮЊ50%ЃЌЗДгІЯћКФСЫ1molвЛбѕЛЏЬМЃЌЯћКФ2molЧтЦјЃЌЪЃгр1molвЛбѕЛЏЬМЃЌЧтЦјЕФЮяжЪЕФСПЮЊ3-2=1molЃЌЩњГЩ1molМзДМЃЌaЕуИїзщЗжЕФХЈЖШЪЧМзДМЕФХЈЖШЮЊ1/2=0.5mol/LЃЌвЛбѕЛЏЬМЕФЮяжЪЕФСПХЈЖШЮЊ1/2=0.5,mol/LЃЌЧтЦјЕФЮяжЪЕФСПХЈЖШЮЊ1/2=0.5mol/LЃЌдђЦНКтГЃЪ§ЮЊ=
ЃЌaЕуЪБЃЌвЛбѕЛЏЬМЕФзЊЛЏТЪЮЊ50%ЃЌЗДгІЯћКФСЫ1molвЛбѕЛЏЬМЃЌЯћКФ2molЧтЦјЃЌЪЃгр1molвЛбѕЛЏЬМЃЌЧтЦјЕФЮяжЪЕФСПЮЊ3-2=1molЃЌЩњГЩ1molМзДМЃЌaЕуИїзщЗжЕФХЈЖШЪЧМзДМЕФХЈЖШЮЊ1/2=0.5mol/LЃЌвЛбѕЛЏЬМЕФЮяжЪЕФСПХЈЖШЮЊ1/2=0.5,mol/LЃЌЧтЦјЕФЮяжЪЕФСПХЈЖШЮЊ1/2=0.5mol/LЃЌдђЦНКтГЃЪ§ЮЊ= ![]() = 4 L2 /mol2
= 4 L2 /mol2
(4)ЗДгІДяЕНЦНКтЪБЃЌИљОнЗДгІЗНГЬЪНПЩжЊИїЮяжЪЕФЮяжЪЕФСПЕФЙиЯЕЃЌвЛбѕЛЏЬМЕФХЈЖШЮЊ0.1-0.04=0.06mol/LЃЌЧтЦјЕФХЈЖШЮЊ0.2-0.08=0.12mol/LЃЌ10ЗжжгЪБвЛбѕЛЏЬМЕФХЈЖШМѕаЁЃЌЧтЦјЕФХЈЖШдіДѓЃЌМзДМЕФХЈЖШдіДѓЃЌдђЦНКтЯђе§ЗДгІЗНЯђвЦЖЏЃЌЕЋЧтЦјЕФХЈЖШдіДѓЃЌЫЕУїИФБфЕФЮяРэСПЮЊдіДѓH2ЕФХЈЖШЃЌЧтЦјЕФХЈЖШдіДѓСЫ0.2-0.12+0.02= 0.1 molL-1ЁЃ

 Н№дПГзЪдОэЯЕСаД№АИ
Н№дПГзЪдОэЯЕСаД№АИЁОЬтФПЁПМзДМЫЎеєЦјжиећжЦЧтЃЈSRMЃЉЪЧгУгкЧ§ЖЏЕчЖЏЦћГЕЕФжЪзгНЛЛЛФЄШМСЯЕчГиЕФРэЯыЧтдДЃЌЕБЧАбаОПжївЊМЏжадкЬсИпДпЛЏМСЛюадКЭНЕЕЭЮВЦјжаCOКЌСПЃЌвдУтЪЙШМСЯЕчГиPtЕчМЋжаЖОЁЃжиећЙ§ГЬЗЂЩњЕФЗДгІШчЯТЃК
ЗДгІI CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g) ІЄH1
CO2(g)+3H2(g) ІЄH1
ЗДгІЂђ CH3OH(g)![]() CO(g)+2H2(g) ІЄH2
CO(g)+2H2(g) ІЄH2
ЗДгІЂѓ CO(g)+H2O(g)![]() CO2(g)+H2(g) ІЄH3
CO2(g)+H2(g) ІЄH3
ЦфЖдгІЕФЦНКтГЃЪ§ЗжБ№ЮЊK1ЁЂK2ЁЂK3ЃЌЦфжаK2ЁЂK3ЫцЮТЖШБфЛЏШчЯТБэЫљЪОЃК
125Ёц | 225Ёц | 325Ёц | |
K2 | 05535 | 1858 | 9939.5 |
K3 | 1577 | 137.5 | 28.14 |
ЧыЛиД№ЃК
ЃЈ1ЃЉЗДгІЂђФмЙЛздЗЂНјааЕФЬѕМў_______ЃЈЬюЁАЕЭЮТЁБЁЂЁАИпЮТЁБЛђЁАШЮКЮЮТЖШЁБЃЉЃЌІЄH1____ІЄH3ЃЈЬюЁА>ЁБЁЂЁА<ЁБЛђЁА=ЁБЃЉЁЃ
ЃЈ2ЃЉЯрЭЌЬѕМўЯТЃЌМзДМЫЎеєЦјжиећжЦЧтНЯМзДМжБНгЗжНтжЦЧтЃЈЗДгІЂђЃЉЕФЯШНјжЎДІдкгк___________________________________________________________________ЁЃ
ЃЈ3ЃЉдкГЃбЙЁЂCat.1ДпЛЏЯТЃЌCH3OHКЭH2OЛьКЭЦјЬхЃЈЬхЛ§БШ1ЁУ1.2ЃЌзмЮяжЪЕФСП2.2molЃЉНјааЗДгІЃЌtlЪБПЬВтЕУCH3OHзЊЛЏТЪМАCOЁЂCO2бЁдёадЫцЮТЖШБфЛЏЧщПіЗжБ№ШчЭМЫљЪОЃЈCOЁЂCO2ЕФбЁдёадЃКзЊЛЏЕФCH3OHжаЩњГЩCOЁЂCO2ЕФАйЗжБШЃЉЁЃ
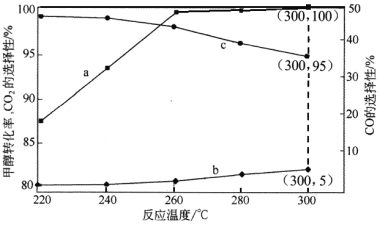
зЂЃКЧњЯпaБэЪОCH3OHЕФзЊЛЏТЪЃЌЧњЯпbБэЪОCOЕФбЁдёадЃЌЧњЯпcБэЪОCO2ЕФбЁдёад
Ђй ЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ__________ЁЃ
AЃЎЗДгІЪЪвЫЮТЖШЮЊ300Ёц
BЃЎЙЄвЕЩњВњЭЈГЃдкИКбЙЬѕМўЯТНјааМзДМЫЎеєЦјжиећ
CЃЎМКжЊCat.2ДпЛЏМСОпгаИќИпДпЛЏЛюадЃЌПЩЬсИпМзДМЦНКтзЊЛЏТЪ
DЃЎЬэМгCaOЕФИДКЯДпЛЏМСПЩЬсИпЧтЦјВњТЪ
Ђк 260ЁцЪБH2ЮяжЪЕФСПЫцЪБМфЕФБфЛЏЧњЯпШчЭМЫљЪОЁЃЛГі300ЁцЪБжСt1ЪБПЬH2ЮяжЪЕФСПЫцЪБМфЕФБфЛЏЧњЯпЁЃ________________
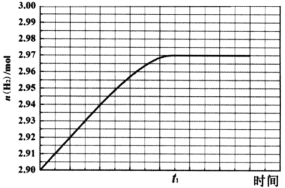
ЃЈ4ЃЉИБВњЮяCO2ПЩвддкЫсадЫЎШмвКжаЕчНтЩњГЩМзЫсЃЌЩњГЩМзЫсЕФЕчМЋЗДгІЪНЪЧЃК___________ЁЃ
ЁОЬтФПЁПИљОнЬтвтЭъГЩЯТСаЮЪЬтЃК
(1)ЙЄвЕЩЯРћгУCOКЭЫЎеєЦјдквЛЖЈЬѕМўЯТЗЂЩњЗДгІжЦШЁЧтЦјЃК
CO(g)ЃЋH2O(g) ![]() CO2(g)ЃЋH2(g) ЁїHЃНЃ41 kJ/mol
CO2(g)ЃЋH2(g) ЁїHЃНЃ41 kJ/mol
вбжЊЃК2H2 (g) + O2 (g) = 2H2O (g) ІЄHЃНЃ484 kJ/molЃЌаДГіCOЭъШЋШМЩеЩњГЩCO2ЕФШШЛЏбЇЗНГЬЪНЃК_______________________________________ЁЃ
(2)ЫцзХДѓЦјЮлШОЕФШеЧїбЯжиЃЌЁАНкФмМѕХХЁБЃЌМѕЩйШЋЧђЮТЪвЦјЬхХХЗХЃЌбаОПNO xЁЂSO2ЁЂCOЕШДѓЦјЮлШОЦјЬхЕФДІРэОпгаживЊвтвхЁЃгУЛюадЬПЛЙдЗЈДІРэЕЊбѕЛЏЮяЃЌгаЙиЗДгІЮЊ:C(s)ЃЋ2NO(g)![]() N2(g)ЃЋCO2(g)ЁЃФГбаОПаЁзщЯђФГУмБеШнЦїМгШывЛЖЈСПЕФЛюадЬПКЭNOЃЌКуЮТ(T1Ёц)ЬѕМўЯТЗДгІЃЌЗДгІНјааЕНВЛЭЌЪБМфВтЕУИїЮяжЪЕФХЈЖШШчЯТЃК
N2(g)ЃЋCO2(g)ЁЃФГбаОПаЁзщЯђФГУмБеШнЦїМгШывЛЖЈСПЕФЛюадЬПКЭNOЃЌКуЮТ(T1Ёц)ЬѕМўЯТЗДгІЃЌЗДгІНјааЕНВЛЭЌЪБМфВтЕУИїЮяжЪЕФХЈЖШШчЯТЃК
ХЈЖШ/molЁЄLЃ1 ЪБМф/min | NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
50 | 0.032 | 0.034 | 0.017 |
ЂйдђДгЗДгІПЊЪМЕН20minЪБЃЌвдNOБэЪОЕФЦНОљЗДгІЫйТЪ= ________ЃЌИУЮТЖШЯТИУЗДгІЕФЦНКтГЃЪ§KЃН____ЃЈБЃСєСНЮЛаЁЪ§ЃЉ
Ђк30minКѓЃЌИФБфФГвЛЬѕМўЃЌЗДгІжиаТДяЕНЦНКтЃЌдђИФБфЕФЬѕМўПЩФмЪЧ_____ЃЈаДвЛЬѕМДПЩЃЉЁЃ
ЂлЯТСаУшЪіжаФмЫЕУїЩЯЪіЗДгІвбДяЦНКтЕФЪЧ__________ЃЛ
AЁЂШнЦїФкЦјЬхЕФЦНОљФІЖћжЪСПБЃГжВЛБф
BЁЂ2v(NO)е§=v(N2)Фц
CЁЂШнЦїжаЦјЬхЕФбЙЧПБЃГжВЛБф
DЁЂЕЅЮЛЪБМфФкЩњГЩnmolCO2ЕФЭЌЪБЩњГЩ2nmolNO
(3)РћгУFe2+ЁЂFe3+ЕФДпЛЏзїгУЃЌГЃЮТЯТНЋSO2зЊЛЏЮЊSO42ЃЃЌ ЖјЪЕЯжSO2ЕФДІРэЃЈзмЗДгІЮЊ2SO2+O2+2H2OЃН2H2SO4ЃЉЁЃвбжЊЃЌКЌSO2ЕФЗЯЦјЭЈШыКЌFe2+ЁЂFe3+ЕФШмвКЪБЃЌЦфжавЛИіЗДгІЕФРызгЗНГЬЪНЮЊ4Fe2+ + O2+ 4H+ ЃН4Fe3+ + 2H2OЃЌдђСэвЛЗДгІЕФРызгЗНГЬЪНЮЊ_______________
(4)габЇепЯывдШчЭМЫљЪОзАжУгУдЕчГидРэНЋSO2зЊЛЏЮЊживЊЕФЛЏЙЄдСЯЁЃ

ШєAЮЊSO2ЃЌBЮЊO2ЃЌCЮЊH2SO4ЃЌдђИКМЋЗДгІЪНЮЊ_______________________________ЃЌЕчГизмЗДгІЪНЮЊ________________________ЁЃ