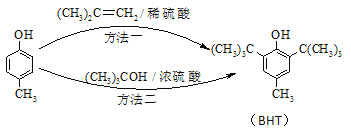
题目内容
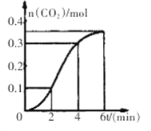
【题目】CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示。下列结论不正确的是
A.反应开始2分钟内平均反应速率最大
B.反应4分钟后平均反应速率最小
C.反应开始4分钟内温度对反应速率的影响比浓度大
D.反应4分钟后反应速率下降的原因是盐酸浓度逐渐减小
【答案】A
【解析】
试题分析:A.根据图示可知在前2分钟内反应产生CO2的物质的量是0.1mol,在2-4分钟内反应产生0.2molCO2,在4-6分钟内反应产生0.1molCO2,所以在第2-4分钟内反应速率最快,错误;B.碳酸钙与盐酸的反应是放热反应,在反应4分钟后由于物质的浓度降低,所以平均反应速率也逐渐减小,由于在相同时间段内反应产生二氧化碳物质的量最小,故该时间段内的反应速率最小,正确;C.碳酸钙与盐酸的反应是放热反应,在开始的不长时间段内,随着反应的进行,溶液的温度逐渐升高,反应速率逐渐加快,根据图示可知在反应开始4分钟内温度对反应速率的影响比浓度大,正确;D.反应4分钟后盐酸浓度降低,反应速率减小,反应速率下降的原因是盐酸浓度逐渐减小,正确。

 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案【题目】一种高分子化合物(VI)是目前市场上流行的墙面涂料之一,其合成路线如下(反应均在一定条件下进行):
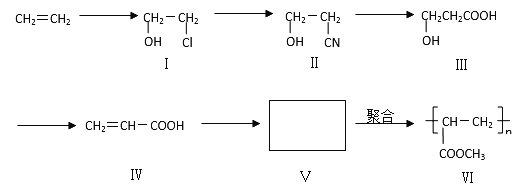
回答下列问题:
(1)目前工业上生产乙烯主要是以 为原料通过 反应来实现。
(2)化合物III生成化合物IV的另外一种产物是 。(提示:该反应的逆反应原子利用率为100%)
(3)写出合成路线中从化合物IV到化合物VI的两步反应的化学方程式: 、 。
(4)下列关于化合物III、IV和V的说法中,正确的是 (填字母)
A.化合物III可以发生氧化反应 |
B.化合物III不可以与NaOH 溶液反应 |
C.化合物IV能与氢气发生加成反应 |
D.化合物III、IV和V均可与金属钠反应生成氢气 |
E.化合物IV和V均可以使溴的四氯化碳溶液褪色