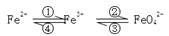题目内容
在由Fe、FeO和Fe2O3组成的混合物中加入100mL 2mol/L的盐酸,恰好使混合物完全溶解,并放出448mL气体(标准状况),此时溶液中无Fe3+。则下列判断正确的是( )
| A.混合物中三种物质反应时消耗盐酸的物质的量之比为1:1:3 |
| B.反应后所得溶液中的Fe2+和Cl-的物质的量之比为1:3 |
| C.混合物中,FeO的物质的量无法确定,但Fe比Fe2O3的物质的量多0.02mol |
| D.混合物中,Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多0.01mol |
C
【错解分析】错选A。混合物计算不要设定比例,注意抓住题中的重要定量关系进行分析判断。错选A是因为默认三者组成为1:1:1,所以要克服这样的思维定势。
【正解】混合物溶解后溶液中无Fe3+,同时有气体生成,所以Fe过量,Fe与Fe2O31:1溶于酸时恰好反应生成Fe2+,过量的铁与酸生成氢气,所以n(Fe)-n(Fe2O3)=n(H2),Fe比Fe2O3的物质的量多0.02mol。

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目