题目内容
【题目】三草酸合铁酸钾晶体{K3[Fe(C2O4)3]·3H2O}易溶于水,难溶于乙醇,可用于摄影和蓝色印刷。三草酸合铁酸钾晶体在110 ℃可完全失去结晶水,继续升高温度可发生分解反应。
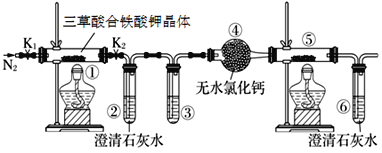
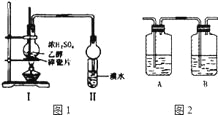
(1)分解得到的气体产物用如下装置进行实验:检查装置气密性后先通一段时间的N2,其目的是_____________;为了实验安全,应先点燃___________________(①或⑤)处的酒精灯;
(2)若③和⑤中分别盛放_____________ 、_______________就可检验生成的CO;
(3)分解得到的固体产物含有K2CO3、FeO、Fe,加水溶解、过滤、洗涤、干燥,得到含铁样品。现设计下列两种实验方案对该样品进行铁元素含量测定:
(甲)a g样品![]() 溶液
溶液![]()
![]() 得固体b g
得固体b g
(乙)a g样品![]() 配制250 mL溶液
配制250 mL溶液![]() ,三次平均消耗0.1 mol·L-1酸性KMnO4溶液V mL.
,三次平均消耗0.1 mol·L-1酸性KMnO4溶液V mL.
你认为以上________(填“甲”或“乙”)方案可确定样品的组成,测得铁元素的含量是__________,不可确定样品组成的方案的理由是_____________________________________。
【答案】排出装置内的空气 ①处酒精灯 足量NaOH溶液 CuO固体 甲 ![]() 乙方案中KMnO4能氧化Cl-,干扰结果
乙方案中KMnO4能氧化Cl-,干扰结果
【解析】
三草酸合铁(Ⅲ)酸钾晶体在110℃可完全失去结晶水,继续升高温度可发生分解反应,根据元素守恒推测得到的产物可能是K2CO3、FeO、Fe、CO2、CO,一氧化碳还原氧化铜,得到的金属铜可被氧气氧化,所以实验开始先通一段时间N2,将装置中的空气排净,实验结束时,为防止倒吸,应该先熄灭酒精灯再通入N2至常温,实验过程中观察到②、⑥中澄清石灰水都变浑浊,即证明二氧化碳产生,⑤中有红色固体生成,证明还原性的气体CO的产生。
(1)检查装置气密性后先通一段时间的N2,其目的是排出装置内的空气;为了实验安全,应先点燃①处酒精灯;
(2)若③中盛放足量NaOH溶液除去分解产生的CO2 ,⑤中盛CuO就可检验生成的CO,实验过程中观察到②、⑥中澄清石灰水都变浑浊,即证明二氧化碳产生,⑤中有红色固体生成,证明还原性的气体CO的产生;
(3)甲中样品溶解过程中亚铁离子被氧化生成铁离子,Fe 3+和OH-反应生成Fe(OH)3沉淀,灼烧沉淀得到固体是Fe2O3,
根据Fe原子守恒得n(Fe)=2n[Fe2O3]=2×![]() =
=![]() mol,
mol,
则样品中Fe元素质量分数=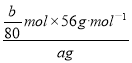 ×100%=
×100%=![]() ;
;
乙不可确定样品组成的方案的理由是:乙方案中KMnO4能氧化Cl-,干扰结果。