题目内容
6.为测定已变质的过氧化钠的纯度,设计如下图所示的实验;Q为一具有良好的弹性气球,称取一定量的样品放于其中,按图安装的实验装置打开分液漏斗的活塞,将稀H2SO4滴入气球中.请填空: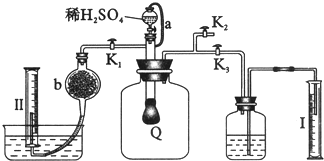
(1)Q内发生反应生成2种气体,其中的反应有1个氧化还原反应.
(2)为测定反应生成气体的总体积,滴稀H2SO4前必须关闭(填K1、K2或K3,下同)K1、K2,打开K3.
(3)当上述反应停止,将K1、K2、K3处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是气球Q慢慢缩小.
(4)导管a的作用是平衡分液漏斗上下的压强使顺利流下.
(5)b中装的固体试剂是碱石灰,为何要缓缓打开K1控制气体流速,使CO2充分吸收.
(6)实验结束时量筒I中有x mL水,量筒II中收集到y mL气体,则过氧化钠的纯度是$\frac{78y}{53x+25y}$(体积折算到标准状况).
分析 (1)变质的过氧化钠中含有碳酸钠,加入酸后Q内发生反应:2Na2O2+2H2SO4=2Na2SO4+2H2O+O2↑;Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,根据化合价变化判断氧化还原反应;
(2)反应产生的CO2、O2使气球变大,将广口瓶中气体排出,水进入量筒Ⅰ中,所以量筒Ⅰ中水的体积即为产生的CO2、O2
的体积;
(3)反应停止,打开K2,再缓缓打开K1,广口瓶内外相通,气球Q慢慢缩小;
(4)为使分液漏斗内液体顺利流下,应是分液漏斗内外压强相等;
(5)混合气体通过碱石灰吸收CO2,最后量筒Ⅱ中收集的是O2;
(6)根据化学方程式计算出碳酸钠、过氧化钠的质量并过氧化钠的纯度.
解答 解:(1)变质的过氧化钠中含有碳酸钠,加入酸后Q内发生反应:2Na2O2+2H2SO4=2Na2SO4+2H2O+O2↑;Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,前者的氧元素的化合价发生了变化,是氧化还原反应,后者元素的化合价未变,是非氧化还原反应,故答案为:2;1;
(2)反应产生的CO2、O2使气球变大,将广口瓶中气体排出,水进入量筒Ⅰ中,所以量筒Ⅰ中水的体积即为产生的CO2、O2的体积,所以滴稀H2SO4前必须关闭K1、K2打开K3,
故答案为:K1、K2;K3;
(3)反应停止,打开K2,再缓缓打开K1,广口瓶内外相通,气球Q慢慢缩小,故答案为:气球Q慢慢缩小;
(4)为使分液漏斗内液体顺利流下,应是分液漏斗内外压强相等,所以导管a的作用是平衡分液漏斗上下的压强使顺利流下,故答案为:平衡分液漏斗上下的压强使顺利流下;
(5)混合气体通过碱石灰吸收CO2,最后量筒Ⅱ中收集的是O2,故答案为:碱石灰;控制气体流速,使CO2充分吸收;
(6)2Na2O2+2H2SO4=2Na2SO4+2H2O+O2↑; Na2CO3 +H2SO4=Na2SO4+H2O+CO2↑,
$\frac{y×10{\;}^{-3}}{22.4}$×2 $\frac{y×10{\;}^{-3}}{22.4}$ $\frac{(x-y)×10{\;}^{-3}}{22.4}$ $\frac{(x-y)×10{\;}^{-3}}{22.4}$
则过氧化钠的质量为:$\frac{y×10{\;}^{-3}}{22.4}$×2×78,碳酸钠的质量为:$\frac{(x-y)×10{\;}^{-3}}{22.4}$×106,
所以过氧化钠的纯度:$\frac{m(过氧化钠)}{m(过氧化钠)+m(碳酸钠)}$=$\frac{78y}{53x+25y}$,故答案为:$\frac{78y}{53x+25y}$.
点评 本题考查混合物含量的测定,题目难度较大,本题要搞清量筒Ⅰ、Ⅱ的作用,根据反应的化学方程式计算即可解答.

 阅读快车系列答案
阅读快车系列答案| A. | 过氧化钠与水反应:2Na2O2+2H2O═4Na++4OH-+O2↑ | |
| B. | 用氢氧化钡溶液中和硫酸溶液:Ba2++OH-+H++SO42-═H2O+BaSO4↓ | |
| C. | 金属钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| D. | 在澄清石灰水中通入过量的CO2:Ca2++2OH-+2CO2═Ca(HCO3)2 |
| A. | HCOOCH2Cl | B. | ClCH2CH2OH | C. | CH2ClCHO | D. | HOCH2CH2OH |
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g).一定温度下,在一个容积不变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是abc(填字母,下同).
a.容器中的压强不变
b.1molH-H 键断裂的同时断裂 2molH-O 键
c.混合气体密度不变
d.c(CO)=c(H2)
(2)将不同量的 CO(g)和 H2O(g)分别通入到体积为 2L 的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到数据如下:
| 起始量/mol | 平衡量/mo l | 达到平衡所 | ||||||
| 需时间/min | ||||||||
| H2O | CO | H2 | CO | |||||
| 2 | 4 | 1.6 | 2.4 | 5 | ||||
(3)目前工业上有一种方法是用 CO2来生产甲醇.一定条件下,在体积为 1L 的恒容密闭容器中,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).为了加快反应速率,可采取什么措施(写两条)升温、使用催化剂.
| A. | 是4He的同素异形体 | B. | 比4He少一个电子 | ||
| C. | 是4He的同位素 | D. | 比4He少一个质子 |
| A. | CO(g)的燃烧热是283.0kJ/mol,则表示CO(g)燃烧反应的热化学方程式为CO(g)+$\frac{1}{2}$O2(g)═CO2(g);△H=-283.0kJ/mol | |
| B. | 稀盐酸和稀氢氧化钠溶液反应的中和热为57.3kJ/mol,则表示稀硫酸与稀氢氧化钾溶液发生反应的热化学方程式为$\frac{1}{2}$H2SO4(l)+KOH(aq)═$\frac{1}{2}$K2SO4(aq)+H2O(l);△H=-57.3kJ/mol | |
| C. | 铝热反应是放热反应,但需要足够的热量才能使反应发生 | |
| D. | CaCO3(s)═CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H>0 |

 .
.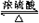 CH3COOC2H5+H2O;反应类型:酯化反应.
CH3COOC2H5+H2O;反应类型:酯化反应.