题目内容
【题目】请完成下列物质的分离提纯问题。
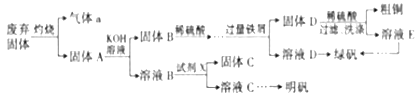
Ⅰ.现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去溶液中的NaCl和Na2SO4,,从而得到纯净的NaNO3溶液。相应的实验过程可用如图表示:

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X__________,沉淀B________。
(2)证明AgNO3溶液加过量的实验方法是___________。
(3)按此实验方案得到的溶液3中肯定含有_____________(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的___________,之后若要获得固体NaNO3需要进行的实验操作是______.(填操作名称)。
Ⅱ.某同学欲用CCl4萃取较高浓度的碘水中的碘,操作过程可以分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50mL碘水和15mLCC14加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层液体;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
H.静置、分层。
(1)萃取过程正确操作步骤的顺序是:______(填编号字母)。
(2)最后碘的CCl4是通过获得________(填“漏斗上口”或“漏斗下口”)。从含碘的CCl4溶液中提取碘和回收CCl4,还需要经过蒸馏,观察下图所示实验装置指出其错误有____________处。
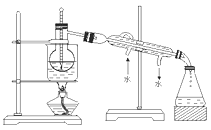
(3)进行上述蒸馏操作时,最后晶态碘在_________(填仪器名称)里聚集。
【答案】Ba(NO3)2或者BaCl2AgCl取滤液或溶液2少许于试管中加入稀盐酸,若产生白色沉淀,证明AgNO3过量Na2CO3HNO3蒸发CBDAHGEF漏斗下口5蒸馏烧瓶
【解析】
I. 除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液,由实验流程可知,若先加入AgNO3,则会同时生成Ag2SO4和AgCl沉淀,所以先加入过量的X为BaCl2[或Ba(NO3)2],生成沉淀A为BaSO4沉淀,然后在溶液1中加入过量的AgNO3,使Cl-全部转化为AgCl沉淀,即沉淀B为AgCl,再向所得溶液2中加入过量的Na2CO3,使溶液中的Ag+、Ba2+完全沉淀,沉淀C为碳酸钡、碳酸银,最后所得溶液3为NaNO3和Na2CO3的混合物,加入稀HNO3,最后进行蒸发操作可得固体NaNO3。
II.萃取分液实验的一般操作步骤为:查漏→装液→振荡→静置→分液等,再根据蒸馏实验原理和物质的性质解答各题。
I.(1). 由上述分析可知,X为Ba(NO3)2或BaCl2,B为AgCl,故答案为:Ba(NO3)2或BaCl2;AgCl;
(2).证明AgNO3加过量的实验方法是取滤液或溶液2少许于试管中,加入稀盐酸,若产生白色沉淀,证明AgNO3过量,故答案为:取滤液或溶液2少许于试管中加入稀盐酸,若产生白色沉淀,证明AgNO3过量;
(3).溶液3为NaNO3和Na2CO3的混合物,加入稀HNO3,可除去Na2CO3,之后蒸发得到硝酸钠,故答案为:Na2CO3;HNO3;蒸发;
II. (1). CCl4从碘水中萃取碘并用分液漏斗分离的操作步骤为:查漏→装液→振荡→静置→分液,正确的顺序为: CBDAHGEF,故答案为:CBDAHGEF;
(2). CCl4从碘水中萃取碘静置分液后,上层液体从上口倒出,下层液体从下口流出,因四氯化碳的密度大于水,所以四氯化碳层应从分液漏斗下口流出;从含碘的CCl4溶液中提取碘和回收CCl4,还需要经过蒸馏,蒸馏时应加入碎瓷片防止爆沸;温度计水银球应放在蒸馏烧瓶支管口处;冷凝水应从下口进入上口流出;尾接管与锥形瓶之间不能有塞子;烧杯加热应垫上石棉网,所以共5处错误,故答案为:漏斗下口; 5;
(3).碘的沸点比四氯化碳沸点高,所以最后晶态碘在蒸馏烧瓶里聚集,故答案为:蒸馏烧瓶。

 每课必练系列答案
每课必练系列答案