题目内容
【题目】氮、磷、砷(As)等VA族元素的化合物在研究和生产中有许多重要用途。
(1)写出基态As原子的核外电子排布式___________________。
(2)NH3、PH3、AsH3熔沸点由高到低的顺序为______。
(3)水合肼(N2H4·H2O)又名水合联氨,是一种重要的化工试剂。利用尿素法生产水合肼的原理为:CO(NH2)2+ 2NaOH+NaClO=Na2CO3+N2H4·H2O+NaCL,该反应中所涉及的第二周期元素第一电离能大小顺序是________。晶体N2H4·H2O中各种微粒间的作用力不涉及__(填字母)。
a:离子键 b.共价键 c.金属键 d.氢键 e.范德华力
(4)NO3-的VSEPR模型是____,H3AsO3分子中As的杂化方式为____。
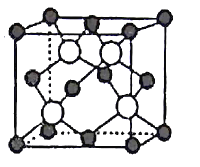
(5)GaAs以第三代半导体著称,性能比硅更优良,广泛用于电子计算机、人造卫星等尖端技术。它的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。GaAs为___ 晶体,晶胞结构与NaCl晶胞____(填“相同”或“不同”)。Ga和As的摩尔质量分别为MGag·mol-l和MAsg·mol-l,原子半径分别为rGapm和rAspm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为___ 。
【答案】 1s22s22p63d104s24p3或[Ar]3d104s24p3 NH3>AsH3>PH3 N>O>C ac 平面三角形 sp2 原子 相同 ![]()
【解析】(1)As为33号元素,基态原子核外电子排布式1s22s22p63d104s24p3或[Ar]3d104s24p3;(2)由于NH3分子间存在氢键,故NH3的熔沸点最高,由于AsH3的相对分子质量大于PH3,故AsH3的熔沸点高于PH3,因此熔沸点由高到低的顺序为NH3>AsH3>PH3;(3)反应CO(NH2)2+ 2NaOH+NaClO=Na2CO3+N2H4·H2O+NaCl中所涉及的第二周期元素有C、N、O,C、N、O属于同一周期元素且原子序数依次减小,同一周期元素的第一电离能随着原子序数的增大而增大,但第ⅤA族的大于第ⅥA族的,所以其第一电离能大小顺序是N>O>C;晶体N2H4·H2O为分子晶体,分子内部存在共价键,与分子间存在氢键和分子间作用力(范德华力),便不涉及离子键和金属键;答案选ac;(4)NO3-中N原子的价层电子对数为![]() =3,则为sp3杂化,没有孤电子对,所以NO3-的VSEPR模型、离子立体构型为平面三角形;根据H3AsO3分子中中心原子As的价层电子对数为
=3,则为sp3杂化,没有孤电子对,所以NO3-的VSEPR模型、离子立体构型为平面三角形;根据H3AsO3分子中中心原子As的价层电子对数为![]() ,所以As原子的杂化方式为sp2杂化;(5)根据GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示,熔点很高,所以GaAs为原子晶体;根据晶胞结构可知晶胞中Ga和As的个数均是4个,晶胞结构与NaCl晶胞相同;晶胞的体积为
,所以As原子的杂化方式为sp2杂化;(5)根据GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示,熔点很高,所以GaAs为原子晶体;根据晶胞结构可知晶胞中Ga和As的个数均是4个,晶胞结构与NaCl晶胞相同;晶胞的体积为![]() ,二者的原子半径分别为rGapm和rAspm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为
,二者的原子半径分别为rGapm和rAspm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为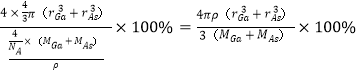 。
。

【题目】钴酸锂(LiCoO2)电池是一种应用广泛的新型电源,电池中含有少量的铝、铁、碳等单质。实验室尝试对废旧钴酸锂电池回收再利用。实验过程如下:
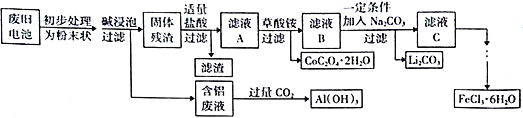
已知:①还原性:Cl->Co2+;
②Fe3+和C2O42-结合生成较稳定的[ Fe(C2O4)3]3-,在强酸性条件下分解重新生成Fe3+。回答下列问题:
(1)废旧电池初步处理为粉末状的目的是________________________________________。
(2)从含铝废液得到Al(OH)3的离子反应方程式为__________________________________。
(3)滤液A中的溶质除HCl、LiCl外还有__________(填化学式)。写出LiCoO2和盐酸反应的化学方程式__________________________________。
(4)滤渣的主要成分为____________________(填化学式)。
(5)在空气中加热一定质量的CoC2O4·2H2O固体样品时,其固体失重率数据见下表,请补充完整表中问题。
已知:①CoC2O4在空气中加热时的气体产物为CO2
②固体失重率=对应温度下样品失重的质量/样品的初始质量
序号 | 温度范围/℃ | 化学方程式 | 固体失重率 |
Ⅰ | 120-220 | CoC2O4·2H2O | 19.67% |
Ⅱ | 300~350 | _________________________ | 59.02% |
(6)已知Li2CO3的溶度积常数Ksp=8.64×10-4,将浓度为0.02mol·L-1的Li2SO4和浓度为0.02 mol·L-1的Na2CO3溶液等体积混合,则溶液中的Li+浓度为___________mol·L-1
(7)从FeCl3溶液得到FeCl3·6H2O固体的操作关键是_________________________。