题目内容
【题目】氮氧化物是形成光化学烟雾和酸雨的重要原因。人们研究了诸多有关氮氧化物的性质,请回答下列问题:
(1)处理 NOx的一种方法是利用甲烷催化还原NOx。
CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) K1
CH4 (g)+2NO2(g) = N2 (g)+CO2(g)+2H2O(g) K2
CH4 (g)+4NO(g) = 2N2 (g)+CO2(g)+2H2O(g) K3
K1、K2、K3依次为三个反应的平衡常数,则K3=______(用K1、K2表示)
(2)在恒容密闭容器中通入等物质的量的CO和NO,在一定条件下发生反应:2CO(g)+2NO(g)![]() N2(g)+2CO2 (g),测得NO的平衡转化率与温度及压强的关系如图所示:
N2(g)+2CO2 (g),测得NO的平衡转化率与温度及压强的关系如图所示:
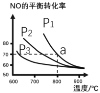
①则该反应的△H ________0(填“﹤”“﹥”或“=”)。
②对于气相反应,用某组分(B)的平衡分压强 p(B)代替物质的量浓度 c(B) 也可表示平衡常数kp,则该反应的平衡常数表达式kp=________,如果p1 =1.65MPa,求a点的平衡常数kp =_________(MPa)1 (结果保留 3 位有效数字,分压=总压×物质的量分数)。
③为探究速率与浓度的关系,该实验中,根据相关实验数据,粗略绘制了2条速率—浓度关系曲线: v正~c(NO)和v逆~c(CO2 )
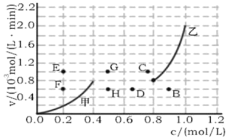
则:与曲线 v正~c(NO)相对应的是图中曲线________(填“甲”或“乙”)。当降低反应体系的温度,反应一段时间后,重新达到平衡,v正和v逆相应的平衡点分别为______(填字母)。
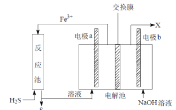
(3)利用电化学原理,将NO2、O2和熔融的KNO3制成燃料电池,模拟工业电解法来处理含Cr2O72的废水,如图所示;电解过程中溶液发生反应:Cr2O72+6Fe2++14H+=2Cr3++6Fe3+ +7H2O。
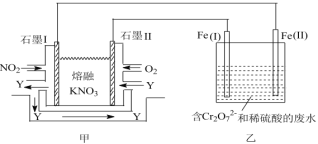
①甲电池工作时,Y是气体,可循环使用。则石墨I附近发生的电极反应式为________。乙池中的pH________(填“变大”“变小”或“不变”)。
②工作时,在相同条件下,甲池内消耗的O2和NO2的体积_____。
(4)已知H3PO4为三元酸,Ka1=7.0×103mol·L1,Ka2=6.2×108 mol·L1,Ka3=4.5×1013mol·L 1。则 Na2HPO4水溶液呈________(填“酸”、“中”、“碱”)性,用Ka与Kh的相对大小,说明判断理由________________。
【答案】![]() ﹤
﹤ ![]() 21.2(MPa)-1 乙 D、H NO2+NO3--e-=N2O5 变大 1:4 碱 Na2HPO4的水解平衡常数Kh2=
21.2(MPa)-1 乙 D、H NO2+NO3--e-=N2O5 变大 1:4 碱 Na2HPO4的水解平衡常数Kh2=![]() =
=![]() =
=![]() =1.6×10—7>Ka3=4.5×1013,HPO42-的水解程度大于电离程度,故而显碱性
=1.6×10—7>Ka3=4.5×1013,HPO42-的水解程度大于电离程度,故而显碱性
【解析】
(1)依据盖斯定律和平衡常数公式换算可得;
(2)①升高温度,平衡向吸热反应方向移动;
②依据反应的平衡常数表达书写即可;由三段式得的物质的物质的量分数,带入公式计算可得;
③NO是反应物,CO2是生成物,随反应进行,NO浓度减小,CO2浓度增大,降低反应体系的温度,v正~c(NO)和v逆~c(CO2 )均减小,该反应为放热反应,平衡向正反应方向移动;
(3)①由题给示意图可知,甲电池工作时,通入二氧化氮的一极为燃料电池的负极;由题给电解方程式可知反应中消耗氢离子,溶液的pH变大;
②根据得失电子守恒计算可得;
(4)Na2HPO4的电离常数和水解常数大小判断Na2HPO4在水溶液的酸碱性。
(1)将已知热化学方程式依次编号为①②③,由盖斯定律可知,②×2-①=③,则K3=![]() ,故答案为:
,故答案为:![]() ;
;
(2)①升高温度,平衡向吸热反应方向移动,由图可知,随温度增大,NO的平衡转化率减小,说明平衡向逆反应方向移动,正反应为放热反应,△H﹤0,故答案为:﹤;
②由反应的化学方程式可知,该反应的平衡常数表达式kp=![]() ;设起始CO和NO的物质的量为1mol,由题给条件可建立如下三段式:
;设起始CO和NO的物质的量为1mol,由题给条件可建立如下三段式:
2CO(g)+2NO(g)![]() N2(g)+2CO2 (g)
N2(g)+2CO2 (g)
起(mol) 1 1 0 0
变(mol) 0.7 0.7 0.35 0.7
平(mol) 0.3 0.3 0.35 0.7
由三段式数据可知,平衡时总物质的量为1.65mol,CO、NO、N2和CO2的平衡分压依次为![]() ×1.65MPa、
×1.65MPa、![]() ×1.65MPa、
×1.65MPa、![]() ×1.65MPa和
×1.65MPa和![]() ×1.65Mpa,则反应的平衡常数表达式kp=
×1.65Mpa,则反应的平衡常数表达式kp=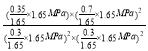 ≈21.2(MPa)-1,故答案为:
≈21.2(MPa)-1,故答案为:![]() ;21.2(MPa)-1;
;21.2(MPa)-1;
③NO是反应物,CO2是生成物,随反应进行,NO浓度减小,CO2浓度增大,则由图可知,与曲线 v正
(3)①由题给示意图可知,甲电池工作时,通入二氧化氮的一极为燃料电池的负极,二氧化氮在负极失电子发生氧化反应生成五氧化二氮,电极反应式为NO2+NO3--e-=N2O5;由电解过程中溶液发生反应为Cr2O72+6Fe2++14H+=2Cr3++6Fe3+ +7H2O可知,反应中消耗氢离子,溶液的pH变大,故答案为:NO2+NO3--e-=N2O5;变大;
②燃料电池工作时,1molO2反应中转移4mol电子,根据得失电子守恒可知,4molNO2转变成N2O5,转移4mol电子,相同状况下气体的体积比等于物质的量之比,故O2和NO2的体积比为1:4,故答案为:1:4;
(4)Na2HPO4在水溶液中发生水解反应,水解平衡为HPO42—+H2O ![]() H2PO4—+OH—,水解平衡常数Kh2=
H2PO4—+OH—,水解平衡常数Kh2=![]() =
=![]() =
=![]() =1.6×10—7>Ka3=4.5×1013,HPO42-的水解程度大于电离程度,故溶液显碱性,故答案为:碱;Na2HPO4的水解平衡常数Kh2=
=1.6×10—7>Ka3=4.5×1013,HPO42-的水解程度大于电离程度,故溶液显碱性,故答案为:碱;Na2HPO4的水解平衡常数Kh2=![]() =
=![]() =
=![]() =1.6×10—7>Ka3=4.5×1013,HPO42-的水解程度大于电离程度,故而显碱性。
=1.6×10—7>Ka3=4.5×1013,HPO42-的水解程度大于电离程度,故而显碱性。