题目内容
【题目】由CO2、CO、H2组成的混合气体在同温同压下与氮气的密度相同,则该混合气体中CO2、H2、CO的体积比可为 ( )
A. 29∶8∶13 B. 22∶1∶14 C. 13∶8∶29 D. 13∶16∶57
【答案】C
【解析】
因为CO与N2具有相同的相对分子质量,所以CO2、CO、H2混合气体的平均相对分子质量仅由CO2和H2来决定,CO的量可以任意,用十字交叉法可以得出结果。
因为CO与N2具有相同的相对分子质量,所以CO2、CO、H2混合气体的平均相对分子质量仅由CO2和H2来决定,CO的量可以任意,由交叉法:
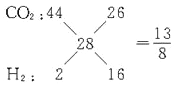
由十字交叉法可求得CO2和H2的体积比为26:16或13:8时(CO的量可以任意),混合气体的平均分子量为28,所以C选项是正确。

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
【题目】类推思维是化学解题中常用的一种思维方法,下列有关反应方程式的类推正确的是
已知 | 类推 | |
A | 将Fe加入CuSO4溶液中Fe+Cu2+===Cu+Fe2+ | 将Na加入到CuSO4溶液中2Na+Cu2+===Cu+2Na+ |
B | 稀硫酸与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-===BaSO4↓+2H2O | NaHSO4溶液与Ba(OH)2溶液反应至中性2H++SO42-+Ba2++2OH-===BaSO4↓+2H2O |
C | 铁和氯气反应2Fe+3Cl2 | 铁和碘单质反应2Fe+3I2 |
D | 向Ca(ClO)2溶液中通入少量CO2:Ca2++2ClO-+CO2+H2O===CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClO |
A. A B. B C. C D. D







